
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
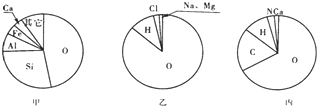 甲、乙、丙分别表示了人体中、海水中、地壳中元素的含量.
甲、乙、丙分别表示了人体中、海水中、地壳中元素的含量.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
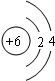 碳与碳的化合物在工农业生产及日常生活中有广泛的用途.
碳与碳的化合物在工农业生产及日常生活中有广泛的用途.查看答案和解析>>
科目: 来源: 题型:解答题
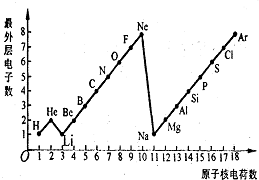 图表是整理数据、发现其中规律的一种重要工具,周期表中1---18号元素最外层电子数与原子序数的关系如图所示,试回答:
图表是整理数据、发现其中规律的一种重要工具,周期表中1---18号元素最外层电子数与原子序数的关系如图所示,试回答:查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
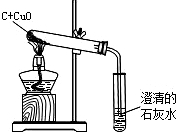 请回忆观察过的“木炭还原氧化铜”的实验,并根据下列教材图示回答问题:
请回忆观察过的“木炭还原氧化铜”的实验,并根据下列教材图示回答问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com