
科目: 来源:2011年初中毕业升学考试(湖南衡阳卷)化学 题型:填空题
(2011年·衡阳)今年我省遭遇近几十年来罕见的大旱,许多地方人畜饮水困难。节约用水,保护水资源是我们每位公民应尽的义务和责任。对于残留在水中的悬浮物(如树叶、废塑料等)可采用 的方法除去。不使用含磷洗衣粉是为了防止水体 。面对水资源短缺的现状,请你写出一种生活中节约用水的方法
。
查看答案和解析>>
科目: 来源:2011年初中毕业升学考试(湖南衡阳卷)化学 题型:填空题
(2011年·衡阳)随着我国工业化进程的加速,有些城市的空气污染较严重。造成空气污染的有害气体有 、氮的氧化物和一氧化碳。氮的氧化物(如NO)主要来自于汽车排放的尾气,在高温条件下氮气(N2)与氧气反应生成一氧化氮,该反应的反应类型是 。一氧化碳和一氧化氮能在催化剂存在的条件下反应生成氮气和二氧化碳,试写该反应的化学方程式 。
查看答案和解析>>
科目: 来源:2011年初中毕业升学考试(湖南衡阳卷)化学 题型:简答题
(2011年·衡阳)由于人类过度使用化石燃料,已造成全球温度升高,异常气候频繁发生。为了减缓全球温室效应增强,各国都在提倡“低碳经济”和“低碳生活”,也就是说在生产和生活中要减少对二氧化碳的排放。请你就如何进行“低碳生活”提出三点建议。
⑶ _______________________。⑵ ________________________________。
⑶_____________________________________。
查看答案和解析>>
科目: 来源:2011年初中毕业升学考试(湖南衡阳卷)化学 题型:简答题
(2011年·衡阳)水电解生成氢气和氧气,并且氢气和氧气的体积比约为1:2。通过水的电解实验(如图所示),我们对所学知识又有了新的认识,请将你的新认识写出三点。
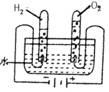
⑴________________________________。
⑵________________________________。
⑶________________________________。
查看答案和解析>>
科目: 来源:2011年初中毕业升学考试(湖南衡阳卷)化学 题型:填空题
(2011年·衡阳)小林同学对A、B、C三种金属的活动性进行探究,他分别将A、B、C三种金属放入三支盛有相同溶质质量分数的稀盐酸中,记录的实验现象为:A、C都能与盐酸反应放出气体,B放入稀盐酸中无明显现象。根据小林同学的记录,你对A、B、C三种金属的活动性能作出的判断是:________、______。不能作出的判断的是_____。要对A、B、C的金属活动性的相对强弱作出准确判断还需要做的实验是___________。
查看答案和解析>>
科目: 来源:2011年初中毕业升学考试(湖南衡阳卷)化学 题型:填空题
(2011年·衡阳)酸碱中和反应在工农业生产和日常生活中应用十分广泛。如下图所示是氢氧化钠与稀盐酸反应的实验示意图。

请据图回答下列问题:
⑴写出图中有标号仪器的名称:① ______ ② __________
⑵A中溶液呈_______色,C中溶液(氢氧化钠溶液稍过量)呈______色。
⑶该实验反应的化学方程式为_________________。
⑶ 璃棒在该实验中的作用是________,其目的是__________。
查看答案和解析>>
科目: 来源:2011年初中毕业升学考试(湖南衡阳卷)化学 题型:探究题
(2011年·衡阳)在学习碳酸钠的性质的课堂上,老师在碳酸钠溶液中加入一定量的澄清石灰水产生白色沉淀,在滤出沉淀后的滤液,引导同学们对滤液中溶质的成分进行探究。同学们通过讨论认为溶质是NaOH、Na2CO3、Ca(OH)2中的一种或两种,其可能情况有三种:①NaOH;②NaOH和Na2CO3;③ 。
小伟同学设计了下列实验方案,请你帮助完成。
|
实 验 步 骤 |
可能出现的实验现象 |
实验结论 |
|
⑴取少量滤液于试管中,加入碳酸钠溶液 |
产生 |
假设③成立 |
|
⑵取少量滤液于试管中,加入足量稀盐酸 |
放出无色气体 |
假设 成立 |
|
⑶取少量滤液于试管中,加入碳酸钠溶液或足量稀盐酸 |
没有明显现象 |
假设 成立 |
小强根据小伟设计的实验方案,在滤液中加入足量稀盐酸,观察到有大量气泡产生,产生该现象化学方程式为 。因此他得出的结论是只有假设 成立,该假设成立说明教师做的实验是 (选填“恰好完全反应”、“Ca(OH)2过量”或“Na2CO3过量”)
查看答案和解析>>
科目: 来源:2011年初中毕业升学考试(湖南衡阳卷)化学 题型:填空题
(2011年·衡阳)某中学课外活动小组在实验室模拟我国化工专家侯德榜先生发明的“联合制碱法”(即“侯氏制碱法”),其原理是向氨化的饱和氯化钠溶液通入足量的二氧化碳,使溶解度较小的碳酸氢钠从溶液中析出,其反应的化学方程式为:NaCl+CO2+NH3+H2O=NH4CI+NaHCO3。该方法不但可以制得纯碱(将NaHCO3进一步处理即可得到纯碱),还得到优质氮肥氯化氨。
试通过计算回答下列问题:
⑴氯化氨中氮元素的质量分数为 _________(计算结果保留0.1%)
⑵实验中得到碳酸氢钠8.4g,求参加反应的氨气质量为多少?
⑶课外活动小组为了这次模拟实验,准备了8.8g二氧化碳,制取这些二氧化碳需要消耗质量分数为10%的稀盐酸的质量为多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com