
科目: 来源: 题型:解答题
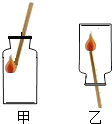 如图,装满氧气的集气瓶,用带火星的木条分别以甲、乙两种方式迅速插入,观察到木条复燃,且在甲中燃烧比在乙中燃烧更旺.上述实验说明了氧气具有性质是:(1)______,(2)______.
如图,装满氧气的集气瓶,用带火星的木条分别以甲、乙两种方式迅速插入,观察到木条复燃,且在甲中燃烧比在乙中燃烧更旺.上述实验说明了氧气具有性质是:(1)______,(2)______.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
| 实验操作 | 实验现象 | 实验结论 | |
| 猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水 | ________ | 猜想a、c不成立,猜想b成立. |
| 探究 | ①用带火星的木条伸入过氧化钠与水反应的试管中 | 木条复燃 | 生成物有________ |
| ②往①试管内的溶液中滴加________ | ________ | 生成物有氢氧化钠 |
查看答案和解析>>
科目: 来源: 题型:解答题
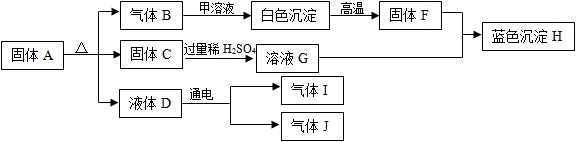
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 Si(粗)+2CO↑
Si(粗)+2CO↑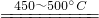 SiCl4
SiCl4 Si(纯)+4HCl
Si(纯)+4HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com