
科目: 来源: 题型:解答题
 已知某金属粉末中除含有Al外还含有一定量的Fe和Cu,为测定其中Al的质量分数,某化学兴趣小组的同学展开了如下的实验探究.资料在线:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2A1+2H2O+2NaOH═2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
已知某金属粉末中除含有Al外还含有一定量的Fe和Cu,为测定其中Al的质量分数,某化学兴趣小组的同学展开了如下的实验探究.资料在线:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2A1+2H2O+2NaOH═2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
取20g该金属粉末,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据与图象:
| 加NaOH溶液的次数 | 第一次 | 第二次 | 第三次 | … |
| 剩余固体的质量/g | 16.5 | n | 9.5 | … |
(1)分析以上数据可知,上表中n的值为______;
(2)该金属粉末中Al的质量分数为______%;
(3)列式计算:所用氢氧化钠溶液的溶质质量分数为多少?(精确到0.1%).
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验步骤 | 实验现象 | 结论或化学方程式 |
| 1.取样,加足量的水, | 固体完全溶解 | |
| 2.用试管取上述试液,加入过量稀硝酸,塞上带导管的单孔塞;将导管的另一端插入______中. | 有______生成, 有______. | 证明原固体烧碱中含有碳酸钠 |
| 3.向试管中再加入______. | 有______生成. | 写出该反应的化学方程式为: ______ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
 某课外活动小组对红褐色铜粉(含炭)样品进行实验,所用装置如图所示(图中部分仪器装置已略去).
某课外活动小组对红褐色铜粉(含炭)样品进行实验,所用装置如图所示(图中部分仪器装置已略去).查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
 (1)用化学符号表示:
(1)用化学符号表示:查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:解答题
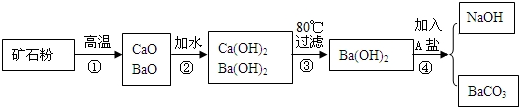
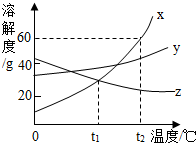
| 温度/℃ 溶解度/g 物质 | 0 | 40 | 80 |
| Ca(OH)2 | 0.187 | 0.141 | 0.094 |
| Ba(OH)2 | 1.67 | 8.22 | 101.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com