
科目: 来源: 题型:解答题
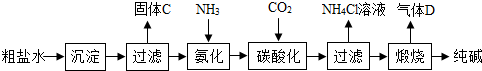
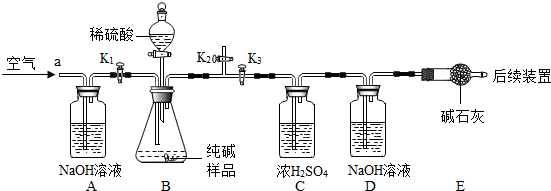
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
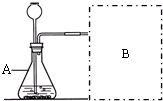 研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题
研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题| 实验编号 | 1 | 2 |
| 反应物 | 6% H2O2 | 6% H2O2 |
| 催化剂 | 1g 红砖粉 | 1g MnO2 |
| 时间 | 152s | 35s |
查看答案和解析>>
科目: 来源: 题型:解答题
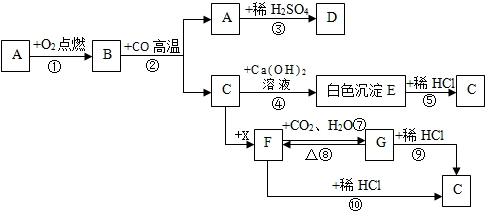
查看答案和解析>>
科目: 来源: 题型:单选题
| 物质 | X | Y | Z | Q |
| 反应前质量(g) | 20 | 2 | 1 | 37 |
| 反应后质量(g) | 未测 | 32 | 1 | 12 |
查看答案和解析>>
科目: 来源: 题型:解答题
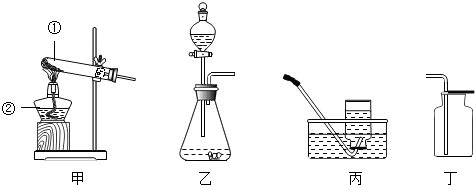
| 比较的方面 | 排水法 | 向上排气法 | 结论 |
| 方法可行性 | O2难溶于水,且不与水反应. | O2的密度比空气______(填“大”或“小”),且不与空气中的物质发生反应. | 两种方法均可行. |
| 收集O2的纯度 | 分别用排水法和向上排空气法收集两瓶氧气(A和B), 放入两支相同的蜡烛,可观察到B瓶内的蜡烛熄灭较早. 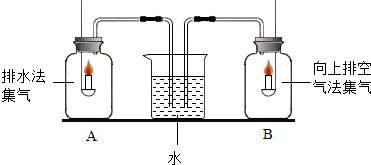 | 结论______. | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com