
【题目】在课堂上,老师演示了金属钠与CuSO4溶液的反应,同学们观察到该反应中生成了蓝色的Cu(OH)2沉淀而没有发现铜单质生成。但某同学想:会不会因生成的铜较少被蓝色沉淀所覆盖而没有被发现呢?于是他想课后到实验室继续探究,希望进一步用实验来验证自己的猜测是否正确。
假如该同学是你,请你写一张实验准备单交给老师,请求老师提供必需的用品。
(1)实验探究的目的是______________________。
(2)探究所依据的化学原理是________________(用必要的文字和化学方程式表示)。
(3)实验必需仪器:小刀、玻璃片、滤纸、____和____;实验药品:金属钠、____和____。该同学在探究实验中意外地发现生成的蓝色沉淀中混有少量的黑色难溶物,而所使用的药品均没有问题,你认为该黑色难溶物是____________,生成该黑色难溶物的原因是________________________________
(用必要的文字和化学方程式表示)。
【答案】(1)确定钠与CuSO4溶液反应是否有铜生成(2分)
(2)氢氧化铜可溶于盐酸而铜不溶,Cu(OH)2+2HCl===CuCl2+2H2O(3分,合理即可)
(3)镊子(1分) 烧杯(1分) CuSO4溶液(1分) 盐酸(或稀硫酸) (1分) CuO(2分) 钠与水反应放出的热使生成的Cu(OH)2部分分解:Cu(OH)2![]() CuO+H2O(3分)
CuO+H2O(3分)
【解析】欲探究钠与CuSO4溶液反应是否置换出铜,应从Cu与Cu(OH)2的不同性质入手探究。最简单的实验是将沉淀分离出来后用盐酸溶解,依此方案可确定所需的仪器和药品。至于黑色难溶物,只可能是CuO,其解释便是Cu(OH)2分解了。实际上,在实验中散热不快,很容易出现此现象。


 阅读快车系列答案
阅读快车系列答案科目:高中地理 来源: 题型:
【题目】以下是表示铁原子和铁离子的3种不同化学用语。
结构示意图 | 电子排布式 | 电子排布图 | |
铁 原 子 |
| 1s22s22p63s23p63d64s2 |
|
铁 离 子 |
| 1s22s22p63s23p63d5 |
|
(1)铁原子最外层电子数为 ,铁在发生化学反应时,参加反应的电子可能是 。
(2)请你通过比较、归纳,分别说出3种不同化学用语所能反映的粒子结构信息。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】甲、乙、丙、丁分别是Na2CO3溶液、AgNO3溶液、BaCl2溶液、盐酸四种无色溶液中的一种,现进行了如图1所示的实验。
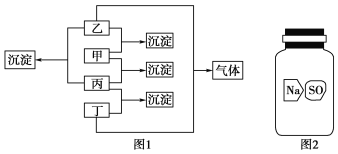
(1)通过上述实验判断出各物质:甲________、乙________、丙________、丁________。写出甲与乙反应的离子方程式______________________。
(2)实验室有一瓶标签破损(如图2所示)的固体试剂。某同学应用(1)中的BaCl2溶液检验,取试剂瓶中的固体少量于试管中,加适量蒸馏水溶解,在所得溶液中加入过量BaCl2溶液,得到白色沉淀。由此,该同学推断这瓶试剂是硫酸钠。你认为他的结论是否正确?________。若正确,请写出相应的离子反应方程式;若不正确,请说明可能的结论,并给出进一步验证的实验方案(要求:所用试剂只能从甲、乙、丙、丁中选用):__________________________________________________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】向2 L密闭容器中通入a mol气体A和b mol气体B,在一定条件下发生反应:xA(g)+yB(g) ![]() pC(g)+qD(g)。已知:平均反应速率vC=
pC(g)+qD(g)。已知:平均反应速率vC=![]() vA;反应2 min时,A的浓度减少了
vA;反应2 min时,A的浓度减少了![]() ,B的物质的量减少了
,B的物质的量减少了![]() mol,有a mol D生成。
mol,有a mol D生成。
回答下列问题:
(1)反应2 min内,vA=________,vB=________。
(2)化学方程式中,x=________,y=__________,p=__________,q=________。
(3)反应平衡时,D为2a mol,则B的转化率为________。
(4)如果只升高反应温度,其他反应条件不变,平衡时D为1.5a mol,则该反应的ΔH________0。(填“>”“<”或“=”)
(5)如果其他条件不变,将容器的容积变为1 L,进行同样的实验,则与上述反应比较:
①反应速率________(填“增大”“减小”或“不变”),理由是____________________________。
②平衡时反应物的转化率________(填“增大”“减小”或“不变”),理由是_________________________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】金属加工后的废切削液中含有2%~5%的NaNO2,它是一种环境污染物。人们用NH4Cl溶液来处理此废切削液,使亚硝酸钠转化为无毒物质。该反应分两步进行:
第一步:NaNO2+NH4Cl===NaCl+NH4NO2
第二步:NH4NO2![]() N2↑+2H2O
N2↑+2H2O
下列对第二步反应的叙述中正确的是
①NH4NO2仅是氧化剂
②NH4NO2仅是还原剂
③NH4NO2发生了分解反应
④只有氮元素的化合价发生了变化
⑤NH4NO2既是氧化剂又是还原剂
A.①④⑤ B.②③④ C.①③⑤ D.③④⑤
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】已知在相同条件下电离常数有如下关系:Ka1(H2CO3)>Ka(HBrO)>Ka2(H2CO3)。下列离子方程式或化学方程式中不正确的是
A.向NaHCO3溶液中滴加少量溴水:![]() +Br2
+Br2![]() HBrO+Br+CO2↑
HBrO+Br+CO2↑
B.向Na2CO3溶液中滴加少量溴水:2![]() +Br2+H2O
+Br2+H2O![]() BrO-+Br-+2
BrO-+Br-+2![]()
C.向NaBrO溶液中通入少量的CO2:CO2+NaBrO+H2O![]() NaHCO3+HBrO
NaHCO3+HBrO
D.向NaBrO溶液中通入足量的CO2:CO2+2NaBrO+H2O![]() Na2CO3+2HBrO
Na2CO3+2HBrO
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】某课外活动小组设计以下装置进行实验:
(1)按如图所示装置进行实验,填写有关现象及化学方程式。
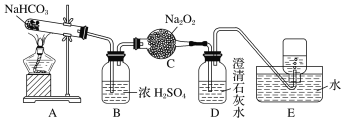
①B中浓硫酸的作用是__________________________________。
②C中发生反应的化学方程式为______________________________________________________。
③D中的现象是___________________________________________。
④E中收集的气体是________。
(2)用如下图所示装置制取纯净的O2。
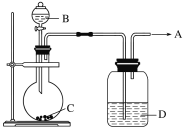
①若C是一种淡黄色固体,则烧瓶中发生反应的化学方程式是______________________。
②若C是一种黑色粉末,则B物质是________,C物质的作用是__________________。
③洗气瓶(广口瓶)中装的试剂D的作用是_____________________。所制得的气体用________法收集。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】某学生为探究AgCl沉淀的溶解和转化,设计实验方案并记录如下:
步骤和现象 | 现象 |
Ⅰ.将等体积等浓度的AgNO3溶液和NaCl溶液混合得到浊液W,过滤,得到滤液X和白色沉淀Y |
|
Ⅱ.向滤液X中滴加几滴饱和Na2S溶液 | 出现浑浊 |
Ⅲ.取少量白色沉淀Y,滴加几滴饱和Na2S溶液 | 沉淀变为黑色 |
Ⅳ.取少量白色沉淀Y,滴加几滴浓氨水 | 沉淀逐渐溶解 |
(1)步骤Ⅰ的浊液W中存在的沉淀溶解平衡为__________________________。
(2)由步骤Ⅱ的浑浊可推测,滤液X中除了含有Na+、NO3,还含有的离子有_________________。
(3)能说明步骤Ⅲ中沉淀变黑的离子方程式为_______________。沉淀转化的主要原因是______________。
(4)已知:Ag+ + 2NH3· H2O ![]() Ag(NH3)2 ++ 2H2O,用平衡移动原理解释步骤Ⅳ中加入浓氨水沉淀逐渐溶解的原因_____________。
Ag(NH3)2 ++ 2H2O,用平衡移动原理解释步骤Ⅳ中加入浓氨水沉淀逐渐溶解的原因_____________。
(5)结合上述信息分析,下列预测不正确的是 。
A.在步骤Ⅳ之后,继续滴加浓硝酸后又有AgCl沉淀生成
B.由步骤Ⅳ可以推测:实验室可用氨水洗涤银镜反应后的试管
C.若在白色沉淀Y中滴加NaOH溶液,沉淀也能溶解
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】 Mr White is too busy to _________ our conversation, so you’d better not ask him.
A. attend B. join
C. join in D. take part in
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com