
【题目】某物质在质谱仪中的最大质荷比为62,该物质的核磁共振氢谱吸收峰共有2组,红外吸收峰表明有O—H键和C—H键。下列物质符合的是( )
A.CH3COOH B.CH3—O—CH2OH
C.CH2OHCH2OH D.CH3—O—CH3
 阅读快车系列答案
阅读快车系列答案科目:高中地理 来源: 题型:
【题目】淀粉溶液是一种胶体,并且淀粉遇到碘单质,可以出现明显的蓝色特征。现将淀粉和稀Na2SO4溶液混合,装在半透膜袋中,浸泡在盛蒸馏水的烧杯内,过一段时间后,取烧杯中液体进行实验,能证明半透膜完好无损的是
A.加入BaCl2溶液产生白色沉淀 B.加入碘水不变蓝
C.加入BaCl2溶液没有白色沉淀产生 D.加入碘水变蓝
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】某共价化合物含C、H、N三种元素,分子内有四个氮原子,且四个氮原子排列成内空的四面体(如白磷的结构),每两个氮原子间都有一个碳原子。已知分子内无碳碳单键,也没有碳碳双键,则该化合物的分子式为( )
A.CH8N4 B.C6H12N4
C.C6H10N4 D.C4H8N4
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】—How about camping this weekend,just for a change?
—OK,___you want
A.whichever
B.however
C.whatever
D.whoever
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】He was a good student and scored___average in most subjects
A.below
B.of
C.on
D.above
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】天津港“8.12”爆炸事故中,因爆炸冲击导致氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻环境污染.
资料:氰化钠化学式NaCN(C元素+2价,N元素﹣3价),白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢.
I、(1)NaCN水溶液呈碱性,其原因是____________(用离子方程式解释).
(2)双氧水氧化法除NaCN:碱性条件下加入H2O2,可得到纯碱和一种无色无味的无毒气体,该反应的离子方程式为____________________________.
(3)非金属性N______C(填“<”、“>”或“=”),请设计实验证明:_____________。
II、某化学兴趣小组实验室制备硫代硫酸钠(Na2S2O3),并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放.
[实验一]实验室通过如图装置制备Na2S2O3.
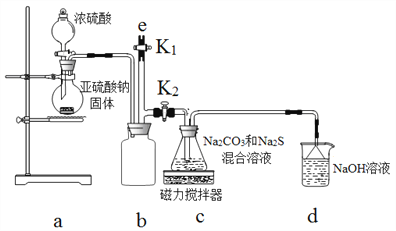
(4)b装置的作用是_______________.
(5)c装置中的产物有Na2S2O3和CO2等,d装置中的溶质有NaOH、Na2CO3,还可能有__.
(6)实验结束后,在e处最好连接盛__(选填“NaOH溶液”、“水”、“CCl4”中任一种)的注射器,再关闭K2打开K1防止拆除装置时污染空气.
[实验二]测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量.
己知:①废水中氰化钠的最高排放标准为0.50mg/L.
②Ag++2CN—=[Ag(CN)2] —,Ag++I—=AgI↓,AgI呈黄色,且CN —优先与Ag+反应.
实验如下.取25.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.000×10﹣4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为2.50mL.
(7)滴定终点的判断方法是_______________.
(8)处理后的废水中氰化钠的含量为_______________mg/L.
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】读我国农业主产区战略布局示意图,回答下列各题。
【1】关于各农业主产区的叙述,正确的是( )
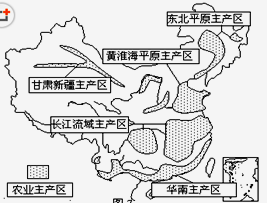
A. 粮食单产最高的是甘肃新疆主产区 B. 土壤最肥沃的是黄淮海平原主产区
C. 光热条件最好的是长江流域主产区 D. 复种指数最高的是华南主产区
【2】优化农业产业布局,重点发展优势产区的意义是( )
①提高市场竞争力 ②推进规模化经营 ③提高专业化水平 ④改善主产区农田生态环境
A. ③④ B. ①②③ C. ②③④ D. ①②③④
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】(1)请用下列10种物质的序号填空:
①O2 ②H2 ③NH4NO3 ④K2O2 ⑤Ba(OH)2 ⑥CH4 ⑦CO2 ⑧NaF ⑨NH3 ⑩I2
其中既有离子键又有非极性键的是________;既有离子键又有极性键的是________。
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,其电子式为________;若XY2为共价化合物时,其结构式为________。
(3)氯化铝的物理性质非常特殊,如:氯化铝的熔点为190 ℃,但在180 ℃就开始升华。据此判断,氯化铝是_______________________(填“共价化合物”或“离子化合物”),可以证明你的判断正确的实验依据是__________________________________________________。
(4)现有a~g 7种短周期元素,它们在周期表中的位置如图所示,请据此回答下列问题:

①元素的原子间反应最容易形成离子键的是________(填序号,下同),容易形成共价键的是________。
A.c和f B.b和g
C.d和g D.b和e
②写出a~g 7种元素形成的所有原子都满足最外层为8电子结构的任意一种分子的分子式____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com