
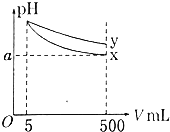
【题目】【2017金华模拟】pH=11的x、y两种碱溶液各5ml,分别稀释至500ml,其pH与溶液体积(V)的关系如图所示,下列说法正确的是( )
A.x是强碱,y是弱碱
B.若x、y是一元碱,则等物质的量浓度的x的硝酸盐溶液的pH比y的硝酸盐溶液大
C.若x、y是一元碱,室温下pH=11的x、y两种碱溶液的浓度相同
D.完全中和x、y两溶液时,消耗同浓度稀硫酸的体积V(x)>V(y)
【答案】B
【解析】A.由图可知,开始的pH相同,两种碱溶液稀释后pH不同,稀释相同的倍数后,X的pH变化较大,所以X的碱性强于Y,但是X不一定是强碱,故A错误;B.若X、Y是一元碱,根据图是得到信息:X的碱性强于Y,根据越弱越水解的原理,则等物质的量浓度的x的硝酸盐溶液的pH比y的硝酸盐溶液大,故B正确;C.由图可知,若X、Y是一元碱,X的碱性强于Y,室温下pH=11的X、Y两种碱溶液的浓度不相同,故C错误;D.由图象可知5mL的溶液中n(OH﹣)关系为Y=X,说明pH=11的X、Y两种碱溶液,溶质浓度Y大于X,完全中和X、Y两溶液时,消耗同浓度硫酸的体积VX<VY,故D错误;故选B。


 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中地理 来源: 题型:
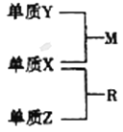
【题目】(云南省曲靖市第一中学2017届高三高考复习质量监测)X、Y、Z是短周期元素,原子半径的大小:r(Y)>r(X)>r(Z),三种元素的原子序数之和为15;X、Y、Z三种元素的常见单质在适当条件下可发生如下图所示转化关系,其中R为10电子分子,是一种常见的无机溶剂。下列说法不正确的是
A. X元素位于周期表中的第16列
B. X的氢化物沸点一定高于Y的氢化物的沸点
C. X、Y、Z元素可以组成一种分子式为Z2Y2X4的化合物,其水溶液中水的电离受到了抑制
D. X、Y、Z元素两两之间均能形成原子个数比为1 : 1的化合物
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】关于高等动物受精作用的叙述,错误的是( )
A.减数分裂产生的卵细胞和精子在受精过程中是随机结合的
B.精卵结合使染色体数目恢复到体细胞数目
C.受精作用中精卵融合利用了细胞膜的结构特点
D.卵细胞同受精卵一样新陈代谢非常旺盛
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】【2017高考江苏】砷(As)是一些工厂和矿山废水中的污染元素,使用吸附剂是去除水中砷的有效措 施之一.
(1)将硫酸锰、硝酸钇与氢氧化钠溶液按一定比例混合,搅拌使其充分反应,可获得一种砷的高效吸附剂X,吸附剂X中含有CO32﹣,其原因是 .
(2)H3AsO3和H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图﹣1和图﹣2所示.
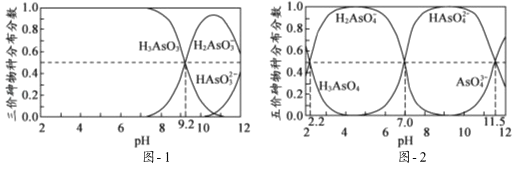
①以酚酞为指示剂(变色范围pH 8.0~10.0),将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加.该过程中主要反应的离子方程式为 .
②H3AsO4第一步电离方程式H3AsO4H2AsO4﹣+H+的电离常数为Ka1,则pKa1= (p Ka1=﹣lg Ka1 ).
(3)溶液的pH对吸附剂X表面所带电荷有影响.pH=7.1时,吸附剂X表面不带电荷; pH>7.1时带负电荷,pH越高,表面所带负电荷越多;pH<7.1时带正电荷,pH越低,表面所带正电荷越多.pH不同时吸附剂X对三价砷和五价砷的平衡吸附量(吸附达平衡时单位质量吸附剂X吸附砷的质量)如图﹣3所示.
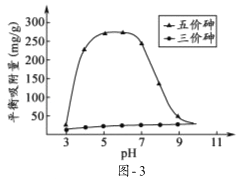
①在pH7~9之间,吸附剂X对五价砷的平衡吸附量随pH升高而迅速下降,其原因是 .
②在pH4~7之间,吸附剂X对水中三价砷的去除能力远比五价砷的弱,这是因为 . 提高吸附剂X对三价砷去除效果可采取的措施是 .
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】位于南极洲麦克默多湾(约78°S)以西的麦克默多干燥谷,大约有200多万年没有降水,是地球上条件最严酷的荒漠,也是南极大陆唯一没有冰雪覆盖的地方。干燥谷中有冰层达数米厚的盐湖。下图为南极洲麦克默多干燥谷景观图。据此完成下列问题。

【1】麦克默多干燥谷降水少的原因是
A. 受极地东风的影响,风力强劲 B. 受高压控制,盛行下沉气流
C. 受寒流影响,降温减湿 D. 受地形影响,地势高
【2】麦克默多干燥谷全年平均气温为-30℃,而冰层下的湖水水温却高达25℃,比较温暖,其主要原因是
A. 湖底地壳活跃,释放大量热能
B. 夏季冰川融水注入,增加了湖水的温度
C. 阳光透过冰层,冰层阻止其热量散失
D. 纬度高终年寒冷,湖水温度变化小
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】【2017榆林一模】常温下,各取1mL,PH=2的,两种二元酸H2A与H2B,分别加水稀释,PH变化与加水稀释倍数有如图所示变化,则下列有关叙述正确的是( )
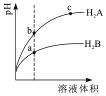
A.H2A的酸性比H2B弱
B.C点溶液的导电性比a、b点溶液的导电性都强
C.若0.1molL﹣1NaHA溶液的PH=4,离子浓度大小为c(Na+)>c(HA﹣)>c(A2﹣)>c(H2A)>c(H+)>c(OH﹣)
D.N2B的水溶液中,离子浓度大小为c(Na+)>c(B2﹣)>c(OH﹣)>c(H+)
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】中国城市正在面临着垃圾围城的困扰。目前天津已建成三座垃圾发电厂,采用先进的空气净化工艺,将垃圾焚烧发电,废渣制砖,余热取暖,形成一个完整的循环产业链,有效地改变传统垃圾处理方式对环境的严重影响。读下图,回答下列各题。
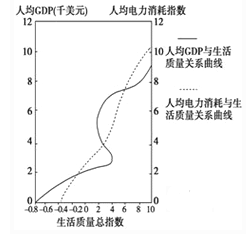
【1】关于建垃圾发电厂对天津的影响()
A. 解决了能紧张状况 B. 改善了城市环境质量
C. 加剧了人地矛盾 D. 冬季取暖完全由余热提供
【2】以下符合可持续发展思想的是()
A. 垃圾分类填埋处理 B. 露天焚烧
C. 分类处理,废弃物再利用 D. 远郊堆放,自然降解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com