
【题目】在稀硫酸、碳酸钠、二氧化碳、铜片、氢氧化钡、氢氧化钠、生石灰、铁片和木炭粉9种物质中,存在下面的相互关系,选择①~⑤为适当的物质,使有连线的两种物质能发生反应。
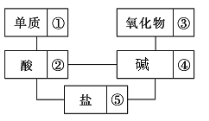
(1)请推断出它们的化学式分别为:
①_______; ②_______; ③________;④________; ⑤_______。
(2)写出下列序号之间反应的化学方程式:
①和②: ____________________________________________;
②和④: ____________________________________________;
②和⑤: ____________________________________________;
④和⑤: ____________________________________________。
【答案】(1)①Fe(1分) ②稀H2SO4(1分) ③CO2(1分) ④Ba(OH)2(1分) ⑤Na2CO3(1分)
(2)Fe+H2SO4![]() FeSO4+H2↑(2分)
FeSO4+H2↑(2分)
H2SO4+Ba(OH)2![]() BaSO4↓+H2O(2分)
BaSO4↓+H2O(2分)
H2SO4+Na2CO3![]() Na2SO4+H2O+CO2↑(2分)
Na2SO4+H2O+CO2↑(2分)
Ba(OH)2 + Na2CO3![]() BaCO3↓+ 2NaOH(2分)
BaCO3↓+ 2NaOH(2分)
【解析】Cu、Fe、C三种单质中,只有Fe能与稀硫酸反应,两者反应生成FeSO4和H2,故①Fe,②为稀H2SO4,碱可能是NaOH、Ba(OH)2 ,盐只有Na2CO3,而NaOH不能与Na2CO3反应,故④为Ba(OH)2,⑤为Na2CO3,③应该为酸性氧化物,即CO2。CO2、CaO氧化物中,只有CaO能与H2SO4反应生成CaSO4,故④为CaO,③为CO2。CaO与H2O反应生成Ca(OH)2 ,Ca(OH)2再与Na2CO3反应生成CaCO3和Na2CO3,故⑤为Na2CO3。H2SO4与Na2CO3反应生成Na2SO4、CO2和H2O。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中地理 来源: 题型:
【题目】完全燃烧一定量的乙烯与某烷烃的混合气体后,测得其生成物中气体的质量是反应前混合烃质量的2.86倍,试通过计算确定该气态烷烃的分子式及它在该混合气体中所占的物质的量分数(气体体积和质量均在常温下测定)。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】化合物YX2、ZX2中X、Y、Z都是前三周期元素,X与Y同周期,Y与Z同主族,Y元素的最外层p轨道上的电子数等于前一电子层电子总数;X原子最外层的p轨道中有一个轨道填充了2个电子。则
(1)X元素基态原子的电子排布式是__________________,Y原子的价层电子的电子排布图是_______________________。
(2)YX2的分子构型是____________。
(3)YX2分子中,Y原子的杂化类型是__________,一个YX2分子中含________个π键。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】食盐晶体是由钠离子和氯离子组成的,且均为等距离的交错排列,如图所示。已知食盐的密度是2.2 g/cm3,阿伏加德罗常数为6.02×1023/mol。在食盐晶体中两个距离最近的钠离子间的距离最接近于 厘米(保留整数)。
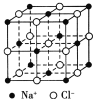
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】铁有许多重要的化合物,除中学化学常见的三种氧化物和两种氢氧化物外,还有许多盐。FeSO4·7H2O是一种浅绿色晶体,俗称绿矾,常用于处理含有氧化性离子的废水。现用绿矾对某工厂废水(含有强氧化性离子![]() )进行处理。
)进行处理。
(1)绿矾除用铁粉与硫酸反应生成外,工业上还可用空气、水、黄铁矿(主要成分为FeS2)来制取。已知该反应除生成硫酸亚铁,还生成一种中学化学常见的强酸,试写出该反应的化学方程式:____________________________。
(2)试配平:_______Fe2++_______![]() +_______ ===_______Fe3++_______Cr3++_______H2O
+_______ ===_______Fe3++_______Cr3++_______H2O
(3)若该废水经处理后Cr3+的含量为1×102 mol·m3,理论上83.4 kg绿矾可以处理该废水________吨(已知废水的密度为1 g·cm3)。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】实验室欲测定某NaOH溶液的物质的量浓度,用0.100 mol·L-1 HCl标准溶液进行中和滴定(用甲基橙作指示剂)。请回答下列问题:
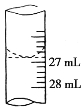
(1)滴定时,盛装待测NaOH溶液的仪器名称为 ,盛装标准盐酸的仪器名称为 ;滴定至终点的颜色变化为 。
(2)甲同学在实验过程中,记录滴定前滴定管内液面读数0.50 mL,滴定后液面如图所示,则此时消耗标准溶液的体积为 。
(3)乙同学做了三组平行实验,数据记录如下:
实验序号 | 待测NaOH溶液的体积/mL | 0.100 mol·L-1 HCl溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.00 | 26.29 |
2 | 25.00 | 1.56 | 31.30 |
3 | 25.00 | 1.00 | 27.31 |
读取上述合理数据,计算出待测NaOH溶液的物质的量浓度为 (保留三位有效数字)。
(4)下列操作会使测定结果偏高的是 (填字母)。
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前酸式滴定管读数正确,滴定后俯视滴定管读数
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】在氯化铁溶液中存在下列平衡:FeCl3+3H2O![]() Fe(OH)3+3HCl ΔH>0。
Fe(OH)3+3HCl ΔH>0。
回答下列问题:
(1)加热FeCl3溶液,溶液的颜色会不断加深,可得到一种红褐色透明液体,向这种液体中加入MgCl2溶液,产生的现象为_________________________。
(2)不断加热FeCl3溶液,蒸干其水分并灼烧得到的固体可能是________。
(3)在配制FeCl3溶液时,为防止浑浊,应加入________。
(4)为了除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入MgCO3固体,过滤后再加入足量盐酸。MgCO3固体能除去Fe3+的原因是______________________________________________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】Fe2O3+2Al![]() Al2O3+2Fe所属基本反应类型是 。在该反应中 元素的化合价升高,该元素的原子 电子,被 。该反应中,Fe2O3发生了 反应,Al发生了 反应, 是氧化剂, 是还原剂, 是氧化产物, 是还原产物。
Al2O3+2Fe所属基本反应类型是 。在该反应中 元素的化合价升高,该元素的原子 电子,被 。该反应中,Fe2O3发生了 反应,Al发生了 反应, 是氧化剂, 是还原剂, 是氧化产物, 是还原产物。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】已知有如图所示物质的相互转化:
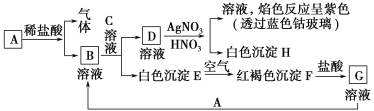
试填写下列空白:
(1)写出B的化学式________,D的化学式________。
(2)写出由E转变成F的化学方程式_______________________________。
(3)写出下列反应的离子方程式:
D溶液与AgNO3溶液反应:________________________________________;
向G溶液中加入A:_____________________________________________。
(4)A与稀盐酸反应生成0.1 mol气体,转移电子数为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com