
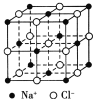
【题目】食盐晶体是由钠离子和氯离子组成的,且均为等距离的交错排列,如图所示。已知食盐的密度是2.2 g/cm3,阿伏加德罗常数为6.02×1023/mol。在食盐晶体中两个距离最近的钠离子间的距离最接近于 厘米(保留整数)。
【答案】4×10-8cm
【解析】解答本题时要注意找出给定的数据与所求量的数据之间的关系。物质的量是联系宏观物理量和微观物理量之间的纽带。即m=ρV=n·M=![]() ·M。食盐晶胞属于立方体结构,所以食盐的一个晶胞中:Na+个数为:8×1/8+6×1/2=4;Cl-个数为:12×1/4+1=4。即每个晶胞中含有4个Na+和4个Cl-,即含4个NaCl结构单元,晶胞的体积就是4个NaCl结构单元的体积。设上述晶胞的边长为2a cm,其体积为8a3 cm3;又已知阿伏加德罗常数个氯化钠结构单元的体积为:(58.5/2.2)cm3。则有:
·M。食盐晶胞属于立方体结构,所以食盐的一个晶胞中:Na+个数为:8×1/8+6×1/2=4;Cl-个数为:12×1/4+1=4。即每个晶胞中含有4个Na+和4个Cl-,即含4个NaCl结构单元,晶胞的体积就是4个NaCl结构单元的体积。设上述晶胞的边长为2a cm,其体积为8a3 cm3;又已知阿伏加德罗常数个氯化钠结构单元的体积为:(58.5/2.2)cm3。则有:![]() =
=![]() ,解得a≈2.8×10-8。
,解得a≈2.8×10-8。
根据晶胞结构图知,距离最近的钠离子之间的距离为晶胞的一个面的面心和顶点之间的距离,设为x,则有:
x2=2a2,解得x≈4×10-8cm。


 智慧小复习系列答案
智慧小复习系列答案科目:高中地理 来源: 题型:
【题目】如图,某气体X可能由H2、CO、CH4中的一种或几种组成。将X气体燃烧,把燃烧后生成的气体通过A、B两个洗气瓶。试回答下列问题:
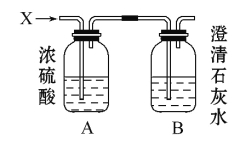
(1)若A洗气瓶的质量增加,B洗气瓶的质量不变,则气体X是 。
(2)若A洗气瓶的质量不变,B洗气瓶的质量增加,则气体X是 。
(3)若A、B两个洗气瓶的质量都增加,试推测X可能有几种组合,填写下表。(有多少种写多少种,不必填满)
组合 | ① | ② | ③ | ④ | ⑤ | ⑥ |
X |
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】下图是元素周期表的简略框架图。
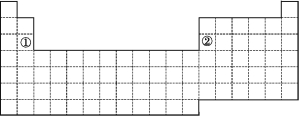
(1)请在上图所示的元素周期表中画出金属元素与非金属元素的分界线。按电子排布,可把元素划分成5个区,不全是金属元素的区为 。
(2)根据氢元素最高正化合价与最低负化合价的绝对值相等,你认为还可把氢元素放在元素周期表中的第 族;有人建议将氢元素排在元素周期表的第ⅦA族,请你写出支持这一观点的一个化学事实: 。
(3)上图中元素①②原子的价电子排布式分别为 、 。
比较元素①与元素②的下列性质(填“>”或“<”)。
原子半径:① ②;电负性:① ②;
金属性:① ②;第一电离能:① ②。
(4)某短周期元素最高正化合价为+7,其原子结构示意图为 。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】甲、乙、丙、丁分别是Na2CO3溶液、AgNO3溶液、BaCl2溶液、盐酸四种无色溶液中的一种,现进行了如图1所示的实验。
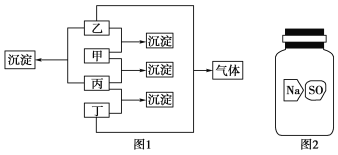
(1)通过上述实验判断出各物质:甲________、乙________、丙________、丁________。写出甲与乙反应的离子方程式______________________。
(2)实验室有一瓶标签破损(如图2所示)的固体试剂。某同学应用(1)中的BaCl2溶液检验,取试剂瓶中的固体少量于试管中,加适量蒸馏水溶解,在所得溶液中加入过量BaCl2溶液,得到白色沉淀。由此,该同学推断这瓶试剂是硫酸钠。你认为他的结论是否正确?________。若正确,请写出相应的离子反应方程式;若不正确,请说明可能的结论,并给出进一步验证的实验方案(要求:所用试剂只能从甲、乙、丙、丁中选用):________________________________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】在水中,水分子可彼此通过氢键形成(H2O)n的小集团。在一定温度下(H2O)n的n=5,每个水分子被4个水分子包围着形成四面体。(H2O)n的n=5时,下列说法中正确的是 ( )

A.(H2O)n是一种新的水分子
B.(H2O)n仍保留着水的化学性质
C.1 mol(H2O)n中有2个氢键
D.1 mol(H2O)n中有4 mol氢键
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】一定温度下,冰醋酸加水稀释过程中溶液的导电能力如图所示。请回答:
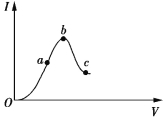
(1)O点为什么不导电___________________________。
(2)a、b、c三点c(H+)由大到小的顺序是______________________________________________。
(3)a、b、c三点中醋酸的电离程度最大的点是________点。
(4)若使c点溶液中的c(CH3COO)提高,可采取的措施是________(填标号)。
A.加热 B.加很稀的NaOH溶液 C.加固体KOH
D.加水 E.加固体CH3COONa F.加锌粉
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】在稀硫酸、碳酸钠、二氧化碳、铜片、氢氧化钡、氢氧化钠、生石灰、铁片和木炭粉9种物质中,存在下面的相互关系,选择①~⑤为适当的物质,使有连线的两种物质能发生反应。
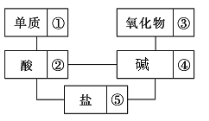
(1)请推断出它们的化学式分别为:
①_______; ②_______; ③________;④________; ⑤_______。
(2)写出下列序号之间反应的化学方程式:
①和②: ____________________________________________;
②和④: ____________________________________________;
②和⑤: ____________________________________________;
④和⑤: ____________________________________________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】(1)常温时向水中加入少量固体MgCl2,________(填“促进”或“抑制”)了水的电离;与纯水相比,所得溶液中KW________(填“变大”“变小”或“不变”)。
(2)现有下列溶液:①20 mL 0.1 mol·L-1 H2SO4溶液;②40 mL 0.1 mol·L-1 CH3COOH溶液;③40 mL 0.1 mol·L-1 HCl溶液;④40 mL 0.1 mol·L-1 NaOH溶液;⑤20 mL 0.1 mol·L-1 Ba(OH)2溶液,其中:
A.c(H+)最小的是________(填序号)
B.任取2份溶液混合,混合溶液的pH为7,有________种取法。
C.②④混合后,溶液的pH________7(填“大于”“小于”或“等于”)。
D.混合后出现白色沉淀的两种溶液是________。(填序号)
(3)常温下,有A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4Cl溶液、盐酸和NaNO3溶液中的一种。已知A、B的水溶液中水的电离程度相同,A、C溶液的pH相同。则:
①B是________溶液,C是________。
②常温下若B溶液中c(OH-)与C溶液中的c(H+)相同,B溶液的pH用pHb表示,C溶液的pH用pHc表示,则pHb+pHc=________(填数据)。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】Fe(OH)2很不稳定,露置在空气中容易被氧化,Fe(OH)2被氧化的化学方程式为:________________________________。
为了获得白色的Fe(OH)2沉淀,可以用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时你觉得还需加入________。
(2)除去蒸馏水中溶解的O2常采用________的方法。
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是_________________________________。
(4)检验Fe3+存在的最佳试剂是____________,现象是______________________________________。
(5)写出Fe与H2O(g)在一定条件下反应的化学方程式:________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com