
【题目】甲~辛等元素在周期表中的相对位置如下表。甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素。下列判断正确的是( )

A.金属性:甲>乙>丁
B.原子半径:辛>己>戊
C.丙和庚的原子核外电子数相差12
D.乙的单质在空气中燃烧生成只含离子键的化合物
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中地理 来源: 题型:
【题目】在100 mL 0.1 mol·L-1的醋酸溶液中,欲使醋酸的电离程度增大,H+浓度减小,可采用的方法是( )
A.加热
B.加入100 mL 0.1 mol·L-1的醋酸溶液
C.加入少量的0.5 mol·L-1的硫酸
D.加入少量的1 mol·L-1的NaOH溶液
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】My teacher told me to___it before I accepted what you gave me
A.think about
B.think twice
C.think up
D.think out
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】《京津冀都市圈区域规划》是国家“十一五”一个重要的区域规划。下为京津冀都市圈区域规划图。回答下列问题。
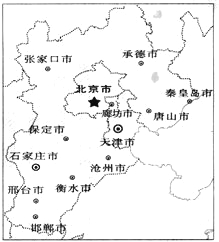
【1】有关“京津冀都市圈”城市规模与服务功能的说法,正确的有
A.北京的城市服务范围最大
B.京、津服务功能属于同一等级
C.廊坊受北京的服务与天津相同
D.天津、石家庄服务范围相等
【2】建设“京津冀都市圈”有利于
A.延缓京、津逆城市化势头 B.扩大北京的城市规模
C.加速钢铁等重工业发展 D.推动京津冀经济一体化
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】图中EF为黑夜与白天的分界线(阴影部分为黑夜);GH为纬线圈的一部分;O点为极点,球面距离CO=AO=2220KM;B为AO中点。读图完成下列各题。
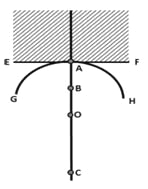
【1】
A. 重庆一中丹桂飘香秋意浓
B. 华北平原冬小麦区一片金黄
C. 一中师生欢歌笑语迎校庆
D. 南非高原草木青翠羚羊成群
【2】
A. 此时,太阳直射点位于(20°S,45°E)
B. 此时,全球新旧两天的比例是8:1
C. B点经度为135°W,其当天正午太阳高度为30°
D. C点经度为45°E,此时的太阳高度为20°
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】下列叙述正确的是
A.直径介于1~100 nm之间的粒子称为胶体
B.用过滤的方法可以将胶体和溶液分离
C.利用丁达尔效应可以区别溶液与胶体
D.胶体区别于其他分散系的本质特征是丁达尔效应
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】Mothers holding jobs outside the home should have___schedules to make it easier to care for their children
A.heavy
B.smooth
C.flexible
D.complex
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】在25 ℃的条件下,将体积都为10 mL,pH都等于3的醋酸和盐酸,加水稀释到a mL和b mL,测得稀释后溶液的pH均为5,则稀释时加入水的体积为( )
A.a=b=10 mL B.a=b>10 mL
C.a<b D.a>b
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】食醋的总酸量即一定体积的食醋原液所含醋酸的质量,单位是g· L-1或个g/100mL。国家标准规定酿造食醋总酸含量不得低于3.5g/100mL。
(1)用酸碱滴定法测定某食醋样品中的总酸量时,下列说法中正确的是 。
A.用NaOH溶液滴定时反应的离子方程式为H++OH-=H2O
B.食醋样品不需要预先稀释一定倍数后可以直接进行滴定
C.用NaOH溶液滴定时,可使用酚酞或甲基橙作指示剂
D.若测得样品的物质的量浓度为0.75mol·L-1,则其总酸量为45g·L-1
(2)某同学仔细观察该食醋样品的标签,发现其中还含有作为食品添加剂的苯甲酸钠(C6H5COONa),他想用理论验证醋酸与苯甲酸钠不会发生离子互换反应,需查找在一定温度下醋酸与苯甲酸的 。
A.pH B.电离度 C.电离常数 D.溶解度
(3)常温下,用0.1000mol· L-1 NaOH溶液分别滴定20.00mL 0.1000mol· L-1 HCl溶液和20.00mL 0.1000mol· L-1 CH3COOH溶液,得到两条滴定曲线,如图所示。

①滴定醋酸溶液的曲线是 (填“图1”或“图2”);滴定曲线中a= mL;
②E点pH>8的原因是(用离子方程式表示): 。
(4)测定食醋的总酸量实验中,配制NaOH溶液和稀释食醋所用的蒸馏水必须煮沸,目的是 。
(5)实验时,吸取食醋样品10mL于100mL容量瓶中定容。移取定容后的溶液20mL于锥形瓶中,加入1~2滴指示剂,用浓度为c mol·L-1的NaOH标准溶液滴定,平行测定三次,消耗NaOH溶液的平均体积为V mL。则原食醋样品的总酸量=____________g/100mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com