
【题目】硬脂酸甘油酯在碱性条件下水解的装置如图所示。进行皂化反应时的步骤如下:
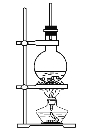
(1)在圆底烧瓶中装入7~8 g硬脂酸甘油酯,然后加入2~3 g的氢氧化钠、5 mL水、10 mL酒精。加入酒精的作用为______________________;
加入NaOH溶液的作用是___________________________。
(2)隔着石棉网给反应混合物加热约10 min,皂化反应基本完成。证明皂化反应进行完全的方法是_______________________。
(3)皂化反应完成后,加入饱和NaCl溶液的作用是____________________。
(4)图中长玻璃导管的作用为________________________。
(5)写出该反应的化学方程式:_________________________。
科目:高中地理 来源: 题型:
【题目】为测定某有机化合物A的结构,进行如下实验:
(一)分子式的确定:
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4 g H2O和8.8 g CO2,消耗氧气6.72 L(标准状况下),则该物质中各元素的原子个数比是_________________。

(2)用质谱仪测定该有机化合物的相对分子质量,得到如图①所示质谱图,则其相对分子质量为________,该物质的分子式是________。
(3)根据价键理论,预测A的可能结构并写出结构简式________。
(二)结构式的确定:
(4)核磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。例如:甲基氯甲基醚(Cl—CH2—O—CH3)有两种氢原子如图②。经测定,有机物A的核磁共振氢谱示意图如图③,则A的结构简式为__________________________。

查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)。请填空:

(1)试管a中需要加入浓硫酸、冰醋酸和乙醇各2 mL,正确的加入顺序及操作是_________________。
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是____________________。
(3)实验中加热试管a的目的是:
①__________________________________;
②__________________________________。
(4)试管b中加有饱和Na2CO3溶液,其作用是______________________。
(5)反应结束后,振荡试管b,静置。观察到的现象是_______________________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】写出下列各烷烃的分子式。
(1)烷烃A在同温同压下蒸气的密度是H2的43倍, 。
(2)烷烃B的分子中含有200个氢原子, 。
(3)分子中含有26个电子的烷烃C, 。
(4)室温下相对分子质量最大的气态直链烷烃D, 。
(5)0.1 mol烷烃E完全燃烧,消耗标准状况下的O211.2 L, 。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】完全燃烧一定量的乙烯与某烷烃的混合气体后,测得其生成物中气体的质量是反应前混合烃质量的2.86倍,试通过计算确定该气态烷烃的分子式及它在该混合气体中所占的物质的量分数(气体体积和质量均在常温下测定)。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】现以C8H18为原料经裂解制得乙烯,进而制得1,2-二溴乙烷,根据如图所示装置,结合有关知识回答问题:
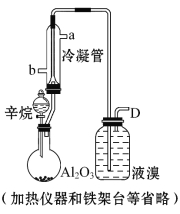
(1)生成乙烯的化学方程式为 , 。
(2)生成1,2-二溴乙烷的化学方程式是 。
(3)使用冷凝管的目的是 ,
冷凝管的进、出水方向为 。
(4)设计三种简单的实验证明广口瓶内发生的是加成反应而不是取代反应:
①第一种: 。
②第二种: 。
③第三种: 。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】一种有机物的结构简式为:
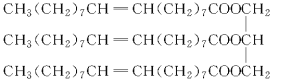
试回答下列问题:
(1)该化合物的种类是________。
A.烯烃 B.酯
C.油脂 D.高分子化合物
(2)该化合物的密度________。
A.比水大 B.比水小
(3)该化合物常温下的状态为________。
A.液体 B.固体 C.气体
(4)与该物质能反应的有________。
A.NaOH溶液
B.碘水
C.乙醇
D.乙酸
E.H2
写出该有机物与选出的化合物反应的化学方程式(任写一个):________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】[2017江苏]铝是应用广泛的金属。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:
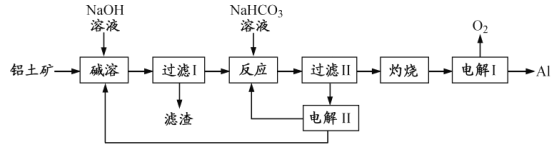
注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为_____________________。
(2)向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,溶液的pH_________ (填“增大”、“不变”或“减小”)。
(3)“电解Ⅰ”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是___________。
(4)“电解Ⅱ”是电解Na2CO3溶液,原理如图所示。阳极的电极反应式为_____________________,阴极产生的物质A的化学式为____________。
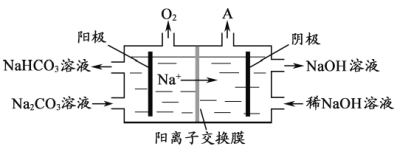
(5)铝粉在1000℃时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是_____________________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】实验室欲测定某NaOH溶液的物质的量浓度,用0.100 mol·L-1 HCl标准溶液进行中和滴定(用甲基橙作指示剂)。请回答下列问题:
(1)滴定时,盛装待测NaOH溶液的仪器名称为 ,盛装标准盐酸的仪器名称为 ;滴定至终点的颜色变化为 。
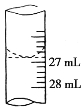
(2)甲同学在实验过程中,记录滴定前滴定管内液面读数0.50 mL,滴定后液面如图所示,则此时消耗标准溶液的体积为 。
(3)乙同学做了三组平行实验,数据记录如下:
实验序号 | 待测NaOH溶液的体积/mL | 0.100 mol·L-1 HCl溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.00 | 26.29 |
2 | 25.00 | 1.56 | 31.30 |
3 | 25.00 | 1.00 | 27.31 |
读取上述合理数据,计算出待测NaOH溶液的物质的量浓度为 (保留三位有效数字)。
(4)下列操作会使测定结果偏高的是 (填字母)。
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前酸式滴定管读数正确,滴定后俯视滴定管读数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com