
科目: 来源: 题型:
【题目】室温下,将0.05 mol Na2CO3固体溶于水配成100mL溶液,向溶液中加入下列物质。有关结论正确的是( )
加入的物质 | 结论 | |
A | 50mL 1 mol·L-1H2SO4 | 反应结束后,c(Na+)=c(SO42-) |
B | 0.05molCaO | 溶液中 |
C | 50mL H2O | 由水电离出的c(H+)·c(OH—)不变 |
D | 0.1molNaHSO4固体 | 反应完全后,溶液pH减小,c(Na+)不变 |
查看答案和解析>>
科目: 来源: 题型:
【题目】298 K时,在20.0 mL 0.10 mol![]() 氨水中滴入0.10 mol
氨水中滴入0.10 mol![]() 的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10 mol
的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10 mol![]() 氨水的电离度为1.32%,下列有关叙述正确的是
氨水的电离度为1.32%,下列有关叙述正确的是
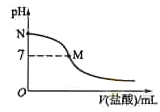
A.该滴定过程应该选择酚酞作为指示剂
B.M点对应的盐酸体积为20.0 mL
C.M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D.N点处的溶液中pH<12
查看答案和解析>>
科目: 来源: 题型:
【题目】TOD模式,是以公共交通为导向的城市用地开发模式。即以公交站点为中心、以400~800米(5~10分钟步行路程)为半径建立集商业、工作、文化教育、居住等为一体的区域中心。如图为“TOD开发模式示意图”,据此完成下面小题。
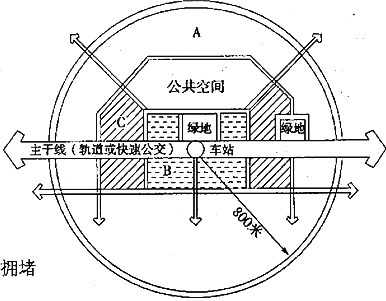
【1】图中A、B、C城市功能区分别为
A. 居住区、核心商业区、办公区 B. 居住区、办公区、核心商业区
C. 核心商业区、办公区、居住区 D. 办公区、核心商业区、居住区
【2】TOD开发模式可以
A. 降低土地利用密度 B. 完全用步行替代公共交通
C. 降低区域人口密度 D. 减少人口“钟摆式”流动导致的交通拥堵
查看答案和解析>>
科目: 来源: 题型:
【题目】The famous scientist grew up___he was born and in 1930 he came to Shanghai
A.wne
B.whenever
C.where
D.wherever
查看答案和解析>>
科目: 来源: 题型:
【题目】John may phone tonight.I don’t want to go out___he phones
A.as long as
B.in order that
C.in case
D.so that
查看答案和解析>>
科目: 来源: 题型:
【题目】为了提纯下列物质(括号内为杂质),所选用的除杂试剂、分离方法、必用仪器都正确的是
选项 | 不纯物质 | 除杂试剂 | 分离方法 | 必用仪器 |
A | 碘水 | 四氯化碳 | 萃取 | 分液漏斗 |
B | 氯化钾(氯化钙) | 适量盐酸 | 过滤 | 玻璃棒 |
C | 硝酸铜(硝酸银) | 适量铜粉 | 结晶 | 酒精灯 |
D | 硫酸钾(碳酸钾) | 适量盐酸 | 蒸馏 | 温度计 |
查看答案和解析>>
科目: 来源: 题型:
【题目】下列分散系最不稳定的是
A.向CuSO4溶液中加入NaOH溶液得到的分散系
B.向水中加入食盐得到的分散系
C.向沸水中滴入FeCl3饱和溶液得到的红褐色液体
D.向NaOH溶液中通入CO2得到的无色液体
查看答案和解析>>
科目: 来源: 题型:
【题目】读非洲某区域图,回答下列各题。
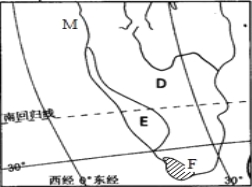
【1】E为纳米布沙漠,它沿非洲西南大西洋海岸延伸2100千米,该沙漠最宽处达160千米,而最狭处只有10千米,其沿海岸线延伸的原因是( )
A.地形 B.降水 C.大气环流 D.洋流
【2】F自然带在此处分布的最高纬度低于35°,其主要的影响因素是( )
A.陆地的纬度分布 B.降水条件 C.地形 D.洋流
查看答案和解析>>
科目: 来源: 题型:
【题目】读下列四岛的相关资料,回答下列各题。
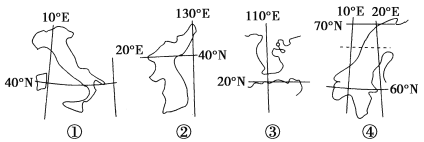
【1】下列说法正确的是 ( )
A.四个半岛均位于板块交界处,故多火山地震
B.四个半岛均临海,故气候均具有海洋性特点
C.半岛②③降水多是因为暖流影响
D.半岛④西侧多峡湾,是冰川侵蚀的结果
【2】下列有关四个半岛气候的叙述,正确的是 ( )
A.半岛②南部为亚热带季风气候,北部为温带季风气候
B.四个半岛均临海,故全年降水丰富
C.半岛①南部为地中海气候,北部为温带海洋性气候
D.半岛④的气候为亚寒带针叶林气候
查看答案和解析>>
科目: 来源: 题型:
【题目】烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:
NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9kJ·mol-1
NO(g)+1/2O2(g)=NO2(g) △H=-58.2kJ·mol-1
SO2(g)+O3(g)=SO3(g)+O2(g) △H=-241.6kJ·mol-1
(1)反应3NO(g)+O3(g)=3NO2(g)的△H=_______mol·L-1。
(2)室温下,固定进入反应器的NO、SO2的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)、n(NO2)和n(SO2)随反应前n(O3):n(NO)的变化见图。
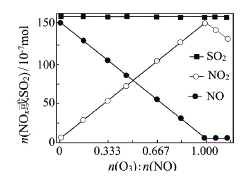
①当n(O3):n(NO)>1时,反应后NO2的物质的量减少,其原因是__________。
②增加n(O3),O3氧化SO2的反应几乎不受影响,其可能原因是 _________。
(3)当用CaSO3水悬浮液吸收经O3预处理的烟气时,清液(pH约为 8)中SO32-将NO2转化为NO2-,其离子方程式为:___________。
(4)CaSO3水悬浮液中加入Na2SO4溶液,达到平衡后溶液中c(SO32-)=________[用c(SO42-)、Ksp(CaSO3)和Ksp(CaSO4)表示];CaSO3水悬浮液中加入Na2SO4溶液能提高NO2的吸收速率,其主要原因是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com