解:(1)FeO、Fe
2O
3溶于硫酸中,会生成硫酸亚铁和硫酸铁,高锰酸钾能将亚铁离子氧化,三价铁遇硫氰酸钾显红的,遇苯酚显紫色,胶头滴管是向试管中滴加试剂的仪器,三价铁遇苯酚显紫色,
故答案为:KSCN或苯酚;胶头滴管;B试管溶液紫色褪去,C试管溶液变红色;
(2)①准确配制一定物质的量浓的溶液可以用容量瓶来配制,准确度高,故答案为:100mL容量瓶;
②具有强氧化性的物质K
2Cr
2O
7溶液应该放在酸式滴定管中,读书精确到小数点后两位,
故答案为:酸式滴定管;100mL容量瓶;
③根据反应6Fe
2++Cr
2O
72-+14H
+=6Fe
3++2Cr
3++7H
2O,可得出6Fe
2+~Cr
2O
72-,消耗 K
2Cr
2O
7溶液体积为25.00mL时,物质的量为:0.0150mol/L×0.025L=0.000375mol,铁矿石中铁元素的百分含量是:
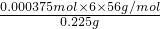
×100%=56%,故答案为:56%;
④a、未用标准K
2Cr
2O
7溶液润洗滴定管,相当于将之稀释,则消耗的标准K
2Cr
2O
7溶液偏多,结果偏高,故a错误;
b.锥形瓶中加入待测溶液后,再加少量水,不影响滴定结果,故b错误;
c.锥形瓶在滴定过程中剧烈摇动,有少量液体溅出,待测液中的溶质减少,则消耗的标准K
2Cr
2O
7溶液偏少,结果偏低,故答案为:c.
分析:(1)三价铁遇硫氰酸钾显红的,遇苯酚显紫色,胶头滴管是向试管中滴加试剂的仪器,高锰酸钾能将亚铁离子氧化,三价铁遇苯酚显紫色;
(2)①准确配制一定物质的量浓度的溶液可以用容量瓶来配制,准确度高;
②具有强氧化性的物质应该放在酸式滴定管中,读书精确到小数点后两位;
③根据反应6Fe
2++Cr
2O
72-+14H
+=6Fe
3++2Cr
3++7H
2O,可得出6Fe
2+~Cr
2O
72-;
④a、未用标准K
2Cr
2O
7溶液润洗滴定管,则消耗的标准K
2Cr
2O
7溶液偏多;
b.锥形瓶中加入待测溶液后,再加少量水,不影响滴定结果;
c.锥形瓶在滴定过程中剧烈摇动,有少量液体溅出,则消耗的标准K
2Cr
2O
7溶液偏少.
点评:本题是一道考查铁的化学性质以及滴定实验的结果误差分析的综合题目,考查角度广,难度大.

 某铁矿石样品除含SiO2外,还含有FeO、Fe2O3中的一种或两种,某同学对铁的氧化物的成分进行探究.
某铁矿石样品除含SiO2外,还含有FeO、Fe2O3中的一种或两种,某同学对铁的氧化物的成分进行探究.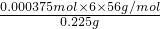 ×100%=56%,故答案为:56%;
×100%=56%,故答案为:56%;

 (2011?天河区一模)某铁矿石样品除含SiO2外,还含有FeO、Fe2O3中的一种或两种,某同学对铁的氧化物的成分进行探究.
(2011?天河区一模)某铁矿石样品除含SiO2外,还含有FeO、Fe2O3中的一种或两种,某同学对铁的氧化物的成分进行探究.