
 ŅŃÖŖÄņĖŲ£Ø½į¹¹¼ņŹ½£ŗ
ŅŃÖŖÄņĖŲ£Ø½į¹¹¼ņŹ½£ŗ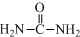 £©æÉÓĆÓŚÖĘÓŠ»śĢś·ŹČżĻõĖįĮłÄņĖŲŗĻĢś£Ø¢ó£©£¬»ÆѧŹ½ĪŖ[Fe£ØH2NCONH2£©6]£ØNO3£©3£®»Ų“šĻĀĮŠĪŹĢā£®
£©æÉÓĆÓŚÖĘÓŠ»śĢś·ŹČżĻõĖįĮłÄņĖŲŗĻĢś£Ø¢ó£©£¬»ÆѧŹ½ĪŖ[Fe£ØH2NCONH2£©6]£ØNO3£©3£®»Ų“šĻĀĮŠĪŹĢā£®·ÖĪö £Ø1£©FeŌ×ÓŗĖĶāµē×ÓŹżĪŖ26£¬ŗĖĶāµē×ÓÅŲ¼ĪŖ1s22s22p63s23p63d64s2£»
£Ø2£©Ķ¬Ņ»ÖÜĘŚŌŖĖŲµÄµŚŅ»µēĄėÄÜĖę×ÅŌ×ÓŠņŹżµÄŌö“ó¶ų³ŹŌö“óµÄĒ÷ŹĘ£¬NH3·Ö×ÓÖŠµŖŹĒsp3Ōӻƣ¬µŖÖÜĪ§ÓŠŅ»¶Ō¹Ā¶Ōµē×Ó¶Ō£»ÄņĖŲ·Ö×ÓŗĶĖ®·Ö×ÓÖ®¼äÄÜŠĪ³ÉĒā¼ü£¬ĖłŅŌÄņĖŲŅ×ČÜÓŚĖ®£»
£Ø3£©Ō×ÓøöŹżĻąµČ¼Ūµē×ÓŹżĻąµČµÄĪ¢Į£ŹĒµČµē×ÓĢ壻
£Ø4£©Ó¦ÓĆ¾łĢÆ·ØČ·¶ØŃõ»ÆĪļµÄ»ÆѧŹ½£®
½ā“š ½ā£ŗ£Ø1£©FeŌ×ÓŗĖĶāÓŠ26øöµē×Ó£¬ŗĖĶāµē×ÓÅŲ¼ĪŖ1s22s22p63s23p63d64s2£¬FeŌ×ÓŹ§Č„4sÄܼ¶2øöµē×Ó”¢3dÄܼ¶1øöµē×ÓŠĪ³ÉFe3+£¬Fe3+µē×ÓÅŲ¼Ź½ĪŖ1s22s22p63s23p63d5£¬¹Ź“š°øĪŖ£ŗ[Ar]3d5£»
£Ø2£©Ķ¬Ņ»ÖÜĘŚŌŖĖŲµÄµŚŅ»µēĄėÄÜĖę×ÅŌ×ÓŠņŹżµÄŌö“ó¶ų³ŹŌö“óµÄĒ÷ŹĘ£¬µ«µŚIIA×åŗĶµŚVA×åŌŖĖŲµÄµŚŅ»µēĄėÄÜ“óÓŚĻąĮŚŌŖĖŲ£¬ĖłŅŌC”¢N”¢OČżÖÖŌŖĖŲµÄµŚŅ»µēĄėÄÜÓɓ󵽊”µÄĖ³ŠņĪŖ£ŗN£¾O£¾C£»NH3·Ö×ÓÖŠµŖŹĒsp3Ōӻƣ¬µŖÖÜĪ§ÓŠŅ»¶Ō¹Ā¶Ōµē×Ó¶Ō£¬ĖłŅŌNH3·Ö×ӵĊĪדŹĒČż½Ē׶ŠĪ£»ÄņĖŲ·Ö×ÓŗĶĖ®·Ö×ÓÖ®¼äÄÜŠĪ³ÉĒā¼ü£¬ĖłŅŌÄņĖŲŅ×ČÜÓŚĖ®£¬¹Ź“š°øĪŖ£ŗN£¾O£¾C£»Čż½Ē׶ŠĪ£» ÄņĖŲ·Ö×ÓŗĶĖ®·Ö×ÓÖ®¼äÄÜŠĪ³ÉĒā¼ü£»
£Ø3£©Ō×ÓøöŹżĻąµČ¼Ūµē×ÓŹżĻąµČµÄĪ¢Į£ŹĒµČµē×ÓĢ壬Ģ¼ĖįøłÓėĻõĖįøłĄė×Ó»„ĪŖµČµē×ÓĢ壬¹Ź“š°øĪŖ£ŗCO32-£»
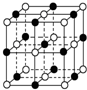
£Ø4£©¾§°ūŹ¾ŅāĶ¼ÖŠĢśŗĶŃõµÄŌ×ÓøöŹż¶¼ŹĒ4£¬ĖłŅŌŃõ»ÆĪļµÄ»ÆѧŹ½ĪŖ£ŗFeO£¬¹Ź“š°øĪŖ£ŗFeO£®
µćĘĄ ±¾ĢāŹĒ¶ŌĪļÖŹ½į¹¹µÄ漲飬Ö÷ŅŖæ¼²é¾łĢƷؼ°¾§°ū½į¹¹µÄ¼ĘĖćµČ»ł“”ÖŖŹ¶£¬ÕżČ·ÅŠ¶Ļ¾§Ģå½į¹¹ŹĒ½āĢāµÄ¹Ų¼ü£¬×¢ŅāĮ¢Ģå¼øŗĪÖŖŹ¶ŌŚ½āĢāÖŠµÄĮé»īŌĖÓĆ£¬ÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 31.3 g | B£® | 27.9 g | C£® | 25.6 g | D£® | 19.8 g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ī¢Į£°ė¾¶ | B£® | »ÆѧŠŌÖŹ | C£® | ×īĶā²ćµē×ÓŹż | D£® | ÖŠ×ÓŹż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | $\frac{12}{13}$ | B£® | $\frac{1}{7}$ | C£® | $\frac{6}{7}$ | D£® | ĪŽ·ØČ·¶Ø |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
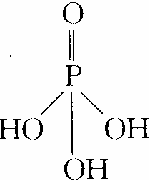 £©£¬Čż¾ŪĮ×ĖįÄĘŹĒ³£ÓƵÄĖ®“¦Ąķ¼Į£¬“ĪĮ×ĖįÄĘ£ØNail2Pa£©æÉÓĆÓŚ»Æѧ¶ĘÄųµČµČ£®Ķź³ÉĻĀĮŠĢīæÕ£ŗ
£©£¬Čż¾ŪĮ×ĖįÄĘŹĒ³£ÓƵÄĖ®“¦Ąķ¼Į£¬“ĪĮ×ĖįÄĘ£ØNail2Pa£©æÉÓĆÓŚ»Æѧ¶ĘÄųµČµČ£®Ķź³ÉĻĀĮŠĢīæÕ£ŗ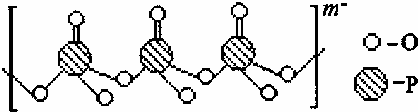
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  µē½ā¾«Į¶ĀĮ | B£® | 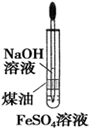 ÖʱøFe£ØOH£©3 | ||
| C£® | 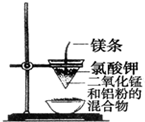 æÉÖĘµĆ½šŹōĆĢ | D£® | 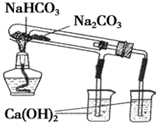 ŃéÖ¤NaHCO3ŗĶNa2CO3µÄČČĪČ¶ØŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅĻ©”¢¼×±½”¢¼×Ķé·Ö×ÓÖŠµÄĖłÓŠŌ×Ó¶¼ŌŚĶ¬Ņ»Ę½ĆęÉĻ | |
| B£® | ³żČ„ŅŅĶéÖŠµÄŅŅĻ©Ź±£¬ĶØČėĒāĘų²¢¼Ó“߻ƼĮ¼ÓČČ | |
| C£® | C3H8µÄ¶žĀČ“śĪļ¹²ÓŠ3ÖÖ | |
| D£® | ŅŅ“¼”¢ŅŅĖį”¢ŅŅĖįŅŅõ„¶¼ÄÜ·¢ÉśČ”“ś·“Ó¦£¬ŅŅĖįŅŅõ„ÖŠµÄÉŁĮæŅŅĖįæÉÓƱ„ŗĶNa2CO3ČÜŅŗ³żČ„ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com