
铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得。
①铝土矿的主要成分是Al2O3和SiO2等。从铝土矿中提炼Al2O3的流程如下:
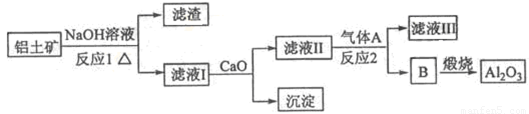
②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如下:

回答下列问题:
(1)写出反应1的化学方程式 ;
(2)滤液Ⅰ中加入CaO生成的沉淀是 ,反应2的离子方程式为 ;
(3)E可作为建筑材料,化合物C是 ,写出由D制备冰晶石的化学方程式 ;
(4)电解制铝的化学方程式是 ,以石墨为电极,阳极产生的混合气体的成分是 。
(1)2NaOH+SiO2=Na2SiO3+H2O(2分) 2NaOH+Al2O3=2NaAlO2+H2O(2分)
(2)CaSiO3(2分) 2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-(2分)
(3)浓H2SO4(1分) 12HF+3Na2CO3+2Al(OH)3=2Na3AlF6+3CO2+9H2O(2分)
(4)2Al2O3 4Al+3O2↑(2分) O2、CO2(CO)(2分)
4Al+3O2↑(2分) O2、CO2(CO)(2分)
【解析】
试题分析:(1)反应1为“碱溶”,发生的反应为:2NaOH+SiO2=Na2SiO3+H2O,2NaOH+Al2O3=2NaAlO2+H2O;(2)滤液I的主要成分是NaAlO2和Na2SiO3,加入生石灰发生的反应:CaO+H2O=Ca(OH)2和Ca(OH)2 +Na2SiO3=CaSiO3+ 2NaOH,即沉淀为CaSiO3。滤液II的主要成分是NaAlO2,通入的气体A是CO2,发生反应的方程式为2NaAlO2+CO2+3H2O=2A l ( O H )3↓+Na2CO3;(3)根据生成物可以作为建筑材料以及加入C能和CaF2 发生反应,可知C是浓硫酸,反应的方程式为CaF2+H2SO4(浓)=CaSO4+2HF;(4)电解法制铝的方程式为2Al2O3 4Al+3O2↑,阳极产生的气体是O2。
4Al+3O2↑,阳极产生的气体是O2。
考点:考查实验基本操作,元素化合物性质及其转化关系,


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.由于铝在常温下不能与氧气反应,所以铝制品具有一定的抗腐蚀性能,是一种应用广泛的金属材料 |
| B.住FeCl3溶液中滴入KI一淀粉溶液,溶液变蓝色 |
| C.元素非金属性Cl>S的实验依据是酸性HCl>H2S |
| D.同周期主族元素的原子形成的简单离子的电子层结构一定相同 |
查看答案和解析>>
科目:高中化学 来源:2011年广东省中山市高考化学模拟试卷(五)(解析版) 题型:选择题
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:单选题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com