
����Ŀ��������ԭ��Ӧ��һ����Ҫ�ķ�Ӧ���밴Ҫ�����������Ŀ��
��1���Է�ӦNH3+O2����NO+H2O(δ��ƽ)���������÷�Ӧ�У�________�ǻ�ԭ����________�ǻ�ԭ�������ԭ��������________��
��2����һ�������£���Ӧ2NH3+3CuO![]() 3Cu+N2+3H2O��˳�����У��Դ˷�Ӧ�ķ�����������________��
3Cu+N2+3H2O��˳�����У��Դ˷�Ӧ�ķ�����������________��
�ٸ÷�Ӧ���û���Ӧ
�ڷ�Ӧ��NH3������ΪN2
���ڷ�Ӧ�������˽���ͭ�Ļ�ԭ��
�ܸ÷�Ӧ��CuO��Ϊ���������뷴Ӧ
��3�� ��ƽ��Ӧ��____H2S+___SO2=____S+____H2O��
���У���������Ϊ________����ԭ��Ϊ________��������Ϊ______��
���𰸡�NH3 NO��H2O O2 �ڢ� 2 1 3 2 S H2S SO2
��������
���ݷ�Ӧ��Ԫ�ػ��ϼ۱仯������ת���غ���ƽ������ԭ��Ӧ���ж�����������ԭ�����������P��ԭ������ݷ�Ӧ�з�Ӧ�P����������ͺ����ʷ�����Ӧ���͡�
(1)�Է�ӦNH3+O2NO+H2O�÷�Ӧ�У������е�Ԫ�ػ��ϼ����ߣ�ʧ���ӣ��������ǻ�ԭ���������õ�����������������ԭ��H2O�ǻ�ԭ���һ����������������ʴ�Ϊ��NH3��NO��H2O�� O2��
(2)��Ӧ2NH3+3CuO![]() 3Cu+N2+3H2O��
3Cu+N2+3H2O��
�ٷ�Ӧ�������ʲμӣ����Ը÷�Ӧ�����û���Ӧ���ʴ���
�ڰ����ǻ�ԭ������Ӧ��NH3������ΪN2��������ȷ��
�۽���ͭ�ǻ�ԭ����ʴ���
��CuO��CuԪ�ػ��ϼ۽��ͣ�����ԭ����������������ȷ���ʴ�Ϊ���ڣ��ܣ�
��3�� ��Ӧ��H2S��SԪ�ػ��ϼ���-2����Ϊ0������ԭ����SO2��SԪ����+4����Ϊ0����������������ת�Ƶ�����Ŀ�غ���ƽ��Ӧ�ã�2H2S+SO2=3S+2H2O�����У���������ΪS����ԭ��ΪH2S��������ΪSO2���ʴ�Ϊ��2 ��1�� 3�� 2�� S�� H2S��SO2��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������з��������Ƶ�������
��MnO2��4HCl(Ũ)![]() MnCl2��Cl2����2H2O
MnCl2��Cl2����2H2O
��KClO3��6HCl(Ũ)===KCl��3Cl2����3H2O
��2KMnO4��16HCl(Ũ)===2KCl��2MnCl2��5Cl2����8H2O
��Ҫ�Ƶ���ͬ�������������٢ڢ۷�Ӧ�е���ת����Ŀ֮��Ϊ�� ��
A. 6��5��6B. 1��3��5C. 15��5��3D. 1��6��10
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ�����(SOCl2)�ڿ��к�ҵ��Ӧ�ñȽϹ㷺���ش��������⣺
I����ҵ������β��SO2��SCl2��Cl2��Ӧ�ϳ��Ȼ��������������·�Ӧ��
��Cl2(g)+SO2(g)![]() SO2Cl2(g) ��H =-471.7kJmol-1
SO2Cl2(g) ��H =-471.7kJmol-1
��SO2Cl2(g)+SCl2(g)![]() 2SOCl2(g) ��H=-5.6kJmol-1
2SOCl2(g) ��H=-5.6kJmol-1
567Kʱ����10L�ܱ������У�����һ������Cl2��SO2��SCl2����ó�ʼѹǿΪP0��Ӧ��������������ѹǿ��P����ʱ�䣨t���仯����Ӧ�ﵽƽ��ʱ���¶�����ʼ�¶���ͬ����ͼ��ʾ����ʼ����ּ���ƽ��ʱSO2Cl2(g)�����ʵ��������

����� | Cl2 | SO2(g) | SCl2(g) | SO2Cl2(g) | SOCl2(g) |
��ʼ/mol | 0.5 | 0.5 | 0.5 | 0 | 0 |
ƽ��/mol | 0.2 |
��1��ͼ��������ʾ0��l min��ϵѹǿ�����ԭ����____��
��2����Ӧ�١��ڴﵽƽ��ʱ��SCl2��ת����Ϊ__��
��3��pK=-lgK��567Kʱ��������Ӧ�ڵ�pK=___(���������λ��Ч���֣���֪lg2=0.30)��
��4��567K�£���ѹ���������Ϊ5L����ƽ��ʱc(SO2)__������ڡ� ��С�ڡ����ڡ���������Ӧƽ��ʱ��c(SO2)��
II.�Ȼ����������ںϳ��������ȡ�������β������װ�õ������а������ʵ���1:1.5Ͷ�ϱȼ�����������Ȼ���������ӦΪCH3CH2CH2COOH+SOCl2![]() CH3CH2CH2COCl+SO2��+HCl����ʵ�����¶Ⱥ�ʱ��Է�Ӧ��Ӱ�������
CH3CH2CH2COCl+SO2��+HCl����ʵ�����¶Ⱥ�ʱ��Է�Ӧ��Ӱ�������
��� | ʵ�鷽�� | ����/% |
1 | 25�棬��Ӧ6h | 73.60 |
2 | 25�棬��Ӧ8h | 74.60 |
3 | 75�棬��Ӧ2h | 75.00 |
4 | 75�棬��Ӧ3h | 76.00 |
5 | ��25�棬��Ӧ1h����75�棬��Ӧ0~1h | 81.10 |
6 | ��25�棬��Ӧ1h����75�棬��Ӧ0~1h | 87.10 |
��5������ʼ�ڽϸ��¶��·�Ӧ�����ų��������塣ͨ�������ϱ����ݣ�ѡ�����ʵ�鷽�������Ϊ___��˵����ѡ��ʵ�鷽�������ɣ�____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�ϳ���ȼ�շ�ȷ���л������ɣ����ַ������ڵ�¯����ʱ�ô���������������Ʒ�����ݲ��������ȷ���л������ɣ���ͼ����װ������ȼ�շ�ȷ���л������ʽ���õ�װ�ã�

�ش��������⣺
��1��������������������������ѡװ�ø����ܵ�����˳���� ��
��2��Cװ����Ũ����������� ��
��3��Dװ����MnO2�������� ��
��4��ȼ�չ���CuO�������� ��
��5����ȷ��ȡ0.90g��Ʒ��ֻ��C��H��O����Ԫ���е����ֻ����֣��������ȼ�պ�A����������1.32g��B����������0.54g������л�������ʽΪ ��
��6��Ҫȷ�����л���ķ���ʽ����Ҫ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25��ʱ��H2R�������ε���Һ�У�H2R��HR-��R2-�ֱ�����������ռ�����ʵ�������(��)����ҺpH�仯��ϵ����ͼ��ʾ������������������
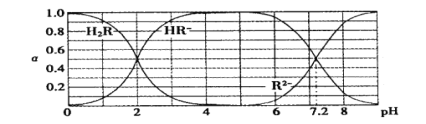
A��H2R�Ƕ�Ԫ���ᣬ��Ka1=1��10-2
B������Һǡ�ó�����ʱ��c( Na + )=2c ( R2- ) + c( HR- )
C��NaHR����Һ��ˮ��������ڵ�������
D����Na2R��NaHR��0.1 mol�Ļ����Һ��pH=7.2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
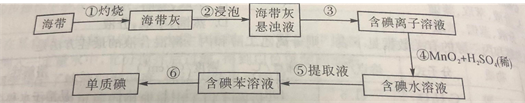
����Ŀ��ʳƷ�㾫������������·��(��Ӧ������ȥ)����

���������������()
A. ����(1)�����в����ı��ӿ���FeCl3��Һ����
B. ���ӺͲ���������������KMnO4��Һ������Ӧ
C. ����(2)�����в�����ϩ����������ˮ����
D. ��������Ͳ�����������NaOH��Һ������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ѧ��ѧ�г����ڻ����ķ�����ᴿ��װ�ã������װ�ûش����⣺
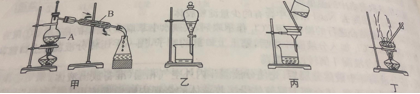
��1��Ϊ�˴Ӻ�������ȡ�⣬ij�о���ѧϰС����Ʋ�����������ʵ�飺
a.���պ���ʱ������Ҫ���ż��⣬����Ҫ�õ�ʵ��������_____������ĸ����
A.�ձ� B.���� C.������ D.������ E.�ƾ��� F.������
b.����۵�ʵ��ѡ������ͼ_____����ס����ҡ�������װ�á�����ݵ�ʵ�����������_____��ѡ������ͼ_____����ס����ҡ�������װ�á������Ŀ���ǴӺ��ⱽ��Һ�з�������ӵ⣬ͬʱ���ձ����ò����ʵ�����������_____��ѡ������ͼ_____����ס����ҡ�������װ�á�
��2��ij�εĻ����Һ�к���Na+��Mg2+��Cl-��SO42-���ӣ����Na+��Mg2+ ��Cl-�����ʵ���Ũ������Ϊ0.2molL-1��0.25molL-1��0.4molL-1����c(SO42-)=_____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ�����������в���ȷ����
A. ��������ΪNA��NO2��CO2��������к��е���ԭ����Ϊ2NA
B. 28 g��ϩ�ͻ�����(C4H8)�Ļ�������к��е�̼ԭ����Ϊ2NA
C. ���³�ѹ�£�92 g��NO2��N2O4������庬�е�ԭ����Ϊ6NA
D. ���³�ѹ�£�22.4 L����������þ�۳�ַ�Ӧ��ת�Ƶĵ�����Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��º��ݵ��ܱ������У�ij���ⷴӦ��MHx(s)+yH2(g)![]() MHx+2y(s) ��H<0�ﵽ��ѧƽ�⡣�����й�������ȷ���ǣ� ��
MHx+2y(s) ��H<0�ﵽ��ѧƽ�⡣�����й�������ȷ���ǣ� ��
A. �����£��÷�Ӧ��ƽ�ⳣ����С
B. ����y mol H2ֻ��1 mol MHx
C. �����������ܶȱ��ֲ���
D. ����������ͨ��������������v(����)>v(����)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com