
����Ŀ����.ʯ����������δ��ϴ���������֣��������о����¹��ɹ����ڱڸ��ŵ��������������ʯ���е���̬�⻯���Ұ�1:3��Ӧ���ɵĺ�ɫ���ʱ���ȼ����ij�о�С�齫һ�����ı���ĩͶ��������Ũ�����з�����Ӧ���õ�4.8g����ɫ�����������ң����ڱ�״���µ��ܶ�Ϊ1.52g��L��1�����˺�����Һ��������ȫ���ݳ����м���������NaOH��Һ���ȳ��ְ�ɫ����������ת��Ϊ���ɫ���������ˡ�ϴ�ӡ����պ�Ĺ�������Ϊ24g����֪�����ҿ�����ˮ��
��ش�
��1������������Ԫ������Ϊ____��
��2�����������з�Ӧ�����ӷ���ʽΪ____��
��3��Ϊ�����������������д�ʩ���е���____��
A. ʯ�����ǰ���� B. ����������ϴ����
C. �����ڱ�Ϳˢ���� D. �����г��뵪��
��. ij��A������Ԫ����ɣ�����ص�ת����ϵ��ͼ�����в�����ѱ��ڿ�ͼ�ϣ�������CΪ����ɫҺ�壬�仯ѧ�����������Ԫ�صĵ������ơ�

��1������B�������ӵĵ���ʽ��____��
��2��������C�������۵���____Ԫ�ء�
��3��������C��KI��Ӧ�Ļ�ѧ����ʽΪ____��
��4�����������У�����C��Ӧ����____��
A. SO2��ˮ��Һ B. H2O C. Na D. Na2SO4
���𰸡� ������ Fe2S3+4H+=2Fe2++S��+2H2S�� AD ![]() I ICl+KI=KCl+I2 ABC
I ICl+KI=KCl+I2 ABC
����������.�����Ũ���ᷴӦ�����Һ(������ȫ���ݳ�)�м���������NaOH��Һ���ȳ��ְ�ɫ����������ת��Ϊ���ɫ����������Һ�к����������ӣ����պ�Ĺ���Ϊ������������Ϊ24g�����������ʵ���Ϊ![]() =0.15mol�����������ʵ���Ϊ0.3mol������ĩͶ��������Ũ�����з�����Ӧ���õ�4.8g����ɫ�����������ң���ɫ����ΪS�����ʵ���Ϊ
=0.15mol�����������ʵ���Ϊ0.3mol������ĩͶ��������Ũ�����з�����Ӧ���õ�4.8g����ɫ�����������ң���ɫ����ΪS�����ʵ���Ϊ![]() =0.15mol�����ڱ�״���µ��ܶ�Ϊ1.52gL-1�����ҵ���Է�������Ϊ1.52��22.4=34�������ҿ�����ˮ������ΪH2S���ڱ�����Ԫ�������ʵ����ʵ���֮��Ϊ2��1���������������̬�⻯���Ұ�1��3��Ӧ���ɵ����ʱ�������Ԫ���غ�͵��ӵ�ʧ�غ���ƶϼ�ΪFe2O3����ΪFe2S3�������ҷ����ķ�Ӧ���ɱ��ķ�ӦΪFe2O3+3H2S=Fe2S3+3H2O�����������з�����ӦΪFe2S3+4HCl=2H2S��+2FeCl2+S��
=0.15mol�����ڱ�״���µ��ܶ�Ϊ1.52gL-1�����ҵ���Է�������Ϊ1.52��22.4=34�������ҿ�����ˮ������ΪH2S���ڱ�����Ԫ�������ʵ����ʵ���֮��Ϊ2��1���������������̬�⻯���Ұ�1��3��Ӧ���ɵ����ʱ�������Ԫ���غ�͵��ӵ�ʧ�غ���ƶϼ�ΪFe2O3����ΪFe2S3�������ҷ����ķ�Ӧ���ɱ��ķ�ӦΪFe2O3+3H2S=Fe2S3+3H2O�����������з�����ӦΪFe2S3+4HCl=2H2S��+2FeCl2+S��
(1)��ΪFe2S3������������Ԫ��Ϊ�����ʴ�Ϊ��������
(2)���������з�Ӧ�����ӷ���ʽΪ��Fe2S3+4H+=2H2S��+2Fe2++S���ʴ�Ϊ��Fe2S3+4H+=2H2S��+2Fe2++S��
(3)A��ʯ�����ǰ����������ֹ��������ɣ���A��ȷ��B������������ϴ���壬��ʹ�ޱڱ䱡�������ڴ����ͣ���B����C�������ڱ�Ϳˢ���ᣬ�������л�������������У�ʹ�ʹ��Ƚ��ͣ���C����D�������г��뵪�����Ϳ��Է�ֹ�ޱ���������Fe2O3����D��ȷ����ѡAD��
��.����ת����ϵ��1molC+KI=1mol������B+1mol����D��1mol������B���������ữ����������Һ��Ӧ���ɰ�ɫ������˵��B�к���ClԪ�أ��ƶ�C�к���ClԪ�أ��������ɵ���D�ƶ�ΪI2��BΪKCl��������������ԭ��Ӧʵ���ж�CΪICl��Ϊ����ɫҺ�壬�仯ѧ�����������Ԫ�صĵ������ƣ�1mol��A�к���Cl��I��K������Ԫ�ػ��ϼ۴�����Ϊ0�жϣ�AΪKICl2��
(1)BΪ�Ȼ��أ�������ΪCl-�������ӵĵ���ʽ��![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
(2)�Ȼ���ṹ���������ƣ�Clԭ�Ӻ�Iԭ��֮�乲��һ�Ե��ӣ�CΪICl���⻯�ϼ�Ϊ+1�ۣ���Ԫ�ػ��ϼ�Ϊ-1�ۣ��ʴ�Ϊ���⣻
(3)C��KI��Ӧ�������ǵ�Ԫ�صĹ��з�Ӧ�����ɵⵥ�ʣ���Ӧ�Ļ�ѧ����ʽΪ��KI+ICl=I2+KCl���ʴ�Ϊ��KI+ICl=I2+KCl��
(4)CΪIClΪ����ɫҺ�壬�仯ѧ�����������Ԫ�صĵ������ƣ�����ǿ�����ԣ���������ԭ�����ʺͲ�����̼ԭ���γɵ�˫�������ӳɷ�Ӧ����ˮ��������������ԭ��Ӧ��A��SO2 B���л�ԭ�Կ��Ա�ICl��������A���ϣ�B������������ˮ��Ӧ����ʽ֪���Ȼ����ˮ��Ӧ����ʽΪICl+H2O�THCl+HIO��H2O��ICl��Ӧ����B���ϣ� C����ϩ���в�����̼̼˫�������������̼̼˫�������ӳɷ�Ӧ����C���ϣ�D��Na2SO4��Һ��ICl���ܷ�����Ӧ����D�����ϣ���ѡABC��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�����ˮ��Ӧ��˵������ȷ����(����)
A. ���κ������£�����ˮ���ܷ�����Ӧ
B. �ڸ���ʱ������ˮ������Ӧ������������������
C. �ڸ���ʱ������ˮ������Ӧ����������������
D. �ڸ���ʱ������ˮ������Ӧ��������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������£���Ӧ��2SO2 ( g ) + O2 ( g ) ![]() 2SO3( g ) ����H =��QkJ��mol��1�����������·ֱ���������ͷ�Ӧ�ų������� ( Q>0 )���±����У�
2SO3( g ) ����H =��QkJ��mol��1�����������·ֱ���������ͷ�Ӧ�ų������� ( Q>0 )���±����У�
�� �� | SO2 (mol) | O2(mol) | N2(mol) | Q(kJ��mol��1) |
�� | 2 | 1 | 0 | Q1 |
�� | 1 | 0.5 | 0 | Q2 |
�� | 1 | 0.5 | 1 | Q3 |
�����������ݣ�����������ȷ����
A. �����������·�Ӧ���� lmolSO3 ������� Q/2 kJ B. 2Q3 <2Q2=Q1<Q
C. Ql =2 Q2= 2Q3 = Q D. 2Q2 = 2Q3 < Q1 < Q
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�Ϊ��ʽ���ڱ���һ���֣����еı�Ŵ�����Ӧ��Ԫ�ء�
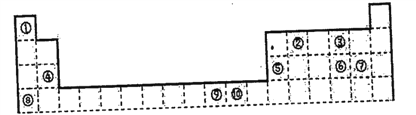
(1)д��Ԫ�آݵ�ԭ�ӹ����ʾʽ______________��
(2)д��Ԫ�آ�Ļ�̬ԭ�ӵļ۵����Ų�ʽ_________��
(3)��������ds����Ԫ����_________(����)
(4)Ԫ�آ��γɵĵ�������____���γɵľ��壬�þ����ȡ�Ķѻ���ʽ��_______�������Т�Ԫ��ԭ�ӵ���λ����_________��
(5)Ԫ���ܡ��ݡ��ޡ��ߵ����Ӱ뾶��С�����˳����_______(�����ӷ��ű�ʾ)
(6)д��Ԫ�آٺ�Ԫ�آ��γɻ�����ĵ���ʽ_________________��
(7)Ԫ�آ����ĵڶ������ֱܷ�Ϊ��I��=1753kJ/mo1��I��=1959kJ/mo1���ڶ�������I�����ԭ����____________________________��
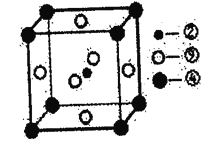
(8)��ѧ�ҷ��֣��ڡ��ܡ�������Ԫ�ص�ԭ���γɵľ�����г����ԣ��侧���Ľṹ�ص�����ͼ��ʾ��ͼ�Тڡ��ܡ���ֱ�λ�ھ��������ġ����㡢���ģ�����û�����Ļ�ѧʽΪ______(�ö�Ӧ��Ԫ�ط��ű�ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�� �����£���20.00 mL 1.000 mol��L��1��ˮ�е���1.000 mol��L��1���ᣬ��ҺpH���¶��������������仯��������ͼ��ʾ�������й�˵���������( )

A�������£�a��İ�ˮ���볣��Ϊ![]()
B�����˰�ˮϡ�ͣ���Һ�ĵ�����������
C��c��ʱ�����������V(HCl)<20 mL
D��a��d�������Һ��ˮ�����ӻ�Kw(a)>Kw(d)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������̬�����Ļ����ڱ�״�������ܶ�Ϊ 1.16 g��L-1������ڸû������ɵ�˵����ȷ����( )
A��һ���м��� B��һ��������
C�������Ǽ���ͼ���Ļ���� D������������ͱ���Ļ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������зḻ��ʳƷ���������Դ��ҩ���ˮ����Դ����ͼΪ��ˮ���õIJ��ֹ��̡������й�˵����ȷ����
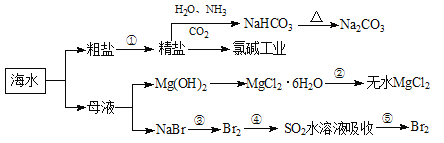
A���������г�ȥ�����е�SO![]() ��Ca2+��Mg2+��Fe3+�����ʣ������Լ���˳��Ϊ��Na2CO3��Һ��NaOH��Һ��BaCl2��Һ�����˺������
��Ca2+��Mg2+��Fe3+�����ʣ������Լ���˳��Ϊ��Na2CO3��Һ��NaOH��Һ��BaCl2��Һ�����˺������
B����ȡNaHCO3�ķ�Ӧ���������ܽ��С��NaCl
C���ӵ��ۢܢ�����Ŀ����Ũ���������嵥�ʣ�����������Ԫ�ؾ�������
D���������нᾧ����MgCl2��6H20���ڿ�����������ˮ�Ƶ���ˮMgCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������CO��N2��H2��CO2������ˮ�����Ļ�����壬����ͨ����������������ͭ��Ũ����������Һ��Ũ�����ʣ���������
A��N2 B��N2��H2 C��N2��C02 D��H2��CO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ij��Ӧ�����淴Ӧ�Ļ�ֱܷ�ΪEakJ/mol��EbkJ/mol�����H=-(Ea-Eb)kJ/mol
B. H2����ֵΪ142.9kJ/g������2H2 (g)+O2(g)=2H2O (l) ��H=-285.8kJ/mol
C. ��Ũ��Ϊ0.1mol/LHF��Һ��ˮ����ϡ�����У�  ʼ�ձ��ּ�С
ʼ�ձ��ּ�С
D. ���ǰ![]() ��������Ļ�Ϻ���Һ�У�
��������Ļ�Ϻ���Һ�У� 
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com