
| A. | OH- | B. | HF | C. | NO | D. | H3O+ |
分析 由于N的质子数为7,H的质子数为1,所以NH4+中质子数为11,电子数为10个.对于电中性原子:质子数=电子数,阳离子:质子数-所带电荷数目=电子数;阴离子:质子数+所带电荷数目=电子数.
解答 解:NH4+中氮原子质子数为7,H原子质子数为1,故NH4+中质子数=7+1×4=11,电子数=11-1=10;
A.OH-中具有9个质子和10个电子,故A错误;
B.HF中具有10个质子和10个电子,故B错误;
C.NO中具有15个质子和15个电子,故C错误;
D.H3O+中具有11个质子和10个电子,故D正确.
故选D.
点评 本题考查微粒中的质子数和电子数,学生应注意中性微粒质子数等于电子数,离子中质子数≠电子数±电荷数,题目难度不大.


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | CH4的稳定性高于SiH4,可推测CH4的沸点也高于SiH4 | |
| B. | 氯化钠的晶格能比氯化铯的晶格能小 | |
| C. | 根据价电子构型与化合价的关系,推出最外层电子数3个的元素一定是第ⅢA族元素 | |
| D. | 根据较强酸可以制取较弱酸的规律,推出SO2通入NaClO溶液中能生成HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
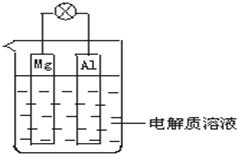 如图所示,试回答下列问题 (灯泡功率合适):
如图所示,试回答下列问题 (灯泡功率合适):查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 温度T下,该反应的平衡常数K=$\frac{({c}_{0}-{c}_{1})^{2}}{{{c}_{1}}^{2}}$ | |
| B. | 若曲线b对应的条件改变是温度,可判断该反应的△H<0 | |
| C. | 曲线b对应的条件改变可能是加入了催化剂 | |
| D. | 温度T下,随着反应的进行,混合气体的密度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上生产水泥和玻璃都要用石灰石做原料 | |
| B. | 玻璃钢是一种合金材料 | |
| C. | 除去氨气中的水蒸气可用无水氯化钙可做干燥剂 | |
| D. | 溶于水可以导电的化合物一定是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 测定这两种溶液的pH值 | B. | 在酸性条件下加入KI淀粉溶液 | ||
| C. | 观察二者的颜色 | D. | 用AgNO3和HNO3两种试剂来区别 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将纯水加热,其KW增大而PH不变 | |
| B. | 常温下,PH=6的溶液一定是酸溶液 | |
| C. | 25℃时,0.1mol/的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱 | |
| D. | 向氨水中加入氯化铵固体会使溶液的pH增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com