
| A. | HCHO | B. | CH3OH | C. | HCOOC2H5 | D. | HCOOCH3 |
分析 核磁共振氢谱中峰值数等于有机物中氢原子的种类数.核磁共振氢谱中只给出一种峰,说明该分子中的H原子都是等效的,只有1种H原子,据此分析.
解答 解:核磁共振氢谱中只给出一种峰,说明该分子中的H原子都是等效的,只有1种H原子.
A.HCHO中2个氢原子连在同一个羰基上,2个H原子都是等效的,核磁共振氢谱中只给出一种峰,故A正确;
B.CH3OH中甲基中的H原子与羟基中的H原子所处化学环境不同,CH3OH有2种H原子,核磁共振氢谱中有2个峰,故B错误;
C.HCOOC2H5中乙基-CH2CH3中的氢原子分为两类,而左边的H原子与乙基-CH2CH3中的H原子所处化学环境也不同,故HCOOC2H5有3种H原子,核磁共振氢谱中有3个峰,故C错误;
D.HCOOCH3中左边H原子与右边中的H原子所处化学环境不同,HCOOCH3有2种H原子,核磁共振氢谱中有2个峰,故D错误.
故选A.
点评 本题考查核磁共振氢谱与有机物中氢原子的种类关系,题目难度不大,核磁共振氢谱中峰值数等于有机物中氢原子的种类数.


科目:高中化学 来源: 题型:解答题
 由铜、锌和稀硫酸组成的原电池中:
由铜、锌和稀硫酸组成的原电池中:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向MgCl2溶液中加入石灰乳:Mg2++2OH-═Mg(OH)2↓ | |
| B. | AlCl3溶液中滴加足量氨水:Al3++4OH-═AlO2-+2H2O | |
| C. | 将SO2通入氯水中:SO2+Cl2+2H2O═SO42-+2Cl-+4H+ | |
| D. | 向Ca(ClO)2溶液中通入过量CO2:2ClO-+CO2+H2O═2HClO+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、Ca2+、Ag+ | B. | Ba2+、Ag+、Ca2+ | C. | Ag+、Ba2+、Ca2+ | D. | Ag+、Ca2+、Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧气的沸点低于氮气的沸点 | |
| B. | 稀有气体原子序数越大沸点越高 | |
| C. | 极性分子中一定不含非极性键 | |
| D. | 乙醇与水任意比互溶只是由于相似相溶原理 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
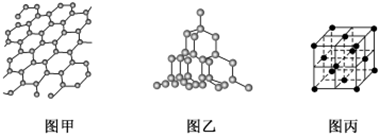
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 40μg/m3 | B. | 80μg/m3 | C. | 100μg/m3 | D. | 160μg/m3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题


 、FCH3CONH2.
、FCH3CONH2. +nHCHO$\stackrel{一定条件}{→}$
+nHCHO$\stackrel{一定条件}{→}$ +nH2O.
+nH2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com