
| A、在Na2A、NaHA两溶液中,离子种类不相同 |
| B、相同浓度的Na2A、NaHA两溶液的pH相等 |
| C、在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-) |
| D、在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-) |


 全能练考卷系列答案
全能练考卷系列答案科目:高中化学 来源: 题型:
| A、反应中Cu2S是还原剂,Cu(NO3)2、CuSO4是氧化产物 |
| B、参加反应的n(Cu2S):n(HNO3)=1:7 |
| C、产物n[Cu(NO3)2]:n[CuSO4]=1:2 |
| D、1 molCu2S参加反应时有10 mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
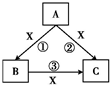 A、B、C、X均为中学化学常见物质,一定条件下它们有如图转化关系(其他产物已略去),回答下列问题:
A、B、C、X均为中学化学常见物质,一定条件下它们有如图转化关系(其他产物已略去),回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Na+、AlO2-、Cl- |
| B、Na+、Cl-、SO42-、HCO3- |
| C、NH4+、Na+、NO3-、SO42- |
| D、Ba2+、Na+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 物质A~D为CH3COOH、NaOH、HCl、NH3?H2O中的各一种,常温下将各种物质的溶液从1mL稀释到1000mL,pH 的变化关系如图所示,请回答下列问题:
物质A~D为CH3COOH、NaOH、HCl、NH3?H2O中的各一种,常温下将各种物质的溶液从1mL稀释到1000mL,pH 的变化关系如图所示,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、因铝对人体有害,故不能使用铝锅等炊具 |
| B、一种治疗胃酸过多的药物的主要成分为Al(OH)3,该药应禁止使用 |
| C、膨化食品中的铝元素超标可能是发酵剂明矾造成的 |
| D、用铝箔包装的茶叶不能食用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
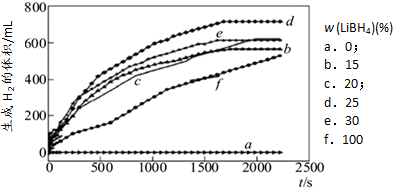
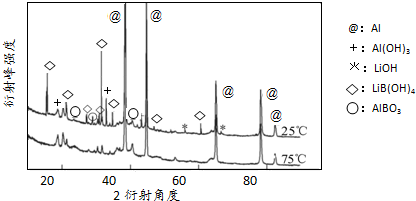
 (g)
(g)| FeSO4/Al2O3 |
| 高温 |
 (g)+)+3H2(g)
(g)+)+3H2(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在江河入海口经常容易形成三角洲 |
| B、明矾用于净水 |
| C、一束平行光线射入蛋白质溶液里,从侧面可以看到一条光亮的通路 |
| D、向煮沸的氢氧化钠溶液滴入饱和FeCl3溶液直至出现红褐色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com