
有A、B、C、D、E五种原子序数增大的元素,只有一种为金属。A、B、C均为第二周期紧邻元素,其第一电离能顺序为B>C>A;B与D同主族;E为第4周期副族元素,其价层电子为全满。
(1)E元素的名称为________,该元素基态原子的价电子排布式为_______。
(2)B与D分别与氢形成最简单氢化物沸点高低顺序为____(用化学式表示);原因_____。
(3)A、B、C三种元素分别与氢形成化合物中的M-M(M代表A、B、C)单键的键能如下表:
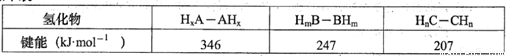
上述三种氢化物中,A、B、C元素原子的杂化方式有_____种;请解释上表中三种氢化物M-M单键的键能依次下降的原因______________________。
(4)D与氯形成的化合物DC15,加压条件下148℃液化,发生完全电离得到一种能够导电的熔体,测定D-Cl键长为198pm和206pm两种,该熔体中含有一种正四面体结构的阳离子,请写出该条件下DC15电离的电离方程式__________;该熔体中阴离子的空间构型为________。
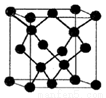
(5)E与C形成的化合物晶体结构有四种,其中一种与金刚石类似,金刚石晶体结构如图所示,该晶体的化学式为______(用元素符号表示);该晶胞的棱长为apm 则该晶体的密度为______g/cm3。
科目:高中化学 来源:2017届河南省天一大联考高三阶段性测试(四)(b卷)理综化学试卷(解析版) 题型:填空题
中国营养学会修订颁布的“每日膳食营养素供给量”将硒(Se)列为15种每日膳食营养素之一,提出一个成年人每天对硒的适宜摄入量是50 ~250μg。回答下列有关问题:
(1) Se 原子的价电子排布式为_______,基态78 Se 原子中,核外存在______对自旋方向相反的电子。
(2)碱金属的硒化物溶液能够溶解硒,生成多硒化合物(M2Sex)。如多硒化钠Na2Se8,该物质中,化学键类型是________,Se原子之间形成的空间构型为_________________。
(3)As、S在元素周期表中均与Se 相邻,其氢化物分别是AsH3、H2Se和H2S其氢化物的稳定性强弱顺序为______________________。
(4)SeCl2和BeCl2均为1:2组成的分子,SeCl2中Se的轨道杂化类型是_______,BeCl2中Be的轨道杂化类型是_________________。
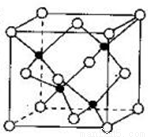
(5)Zn与Se同周期,S与Se同主族。由Zn与S形成的ZnS可用于制白色的颜料及玻璃、发光粉、橡胶、塑料、发光油漆等。ZnS晶胞结构如图所示,黑球代表的原子在晶胞内,白球代表的原子除在顶点外,其余的原子在晶胞_________ (填“内部”“棱上”或“面心”),若该晶体的密度为ρg·㎝-3,阿伏加德罗常数为NA mol-1,则立方晶胞的棱长=_____㎝(用含p、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省南京市高二学业水平模拟测试化学试卷(解析版) 题型:选择题
下列冶炼金属的方法错误的是
A. 电解熔融氧化铝制铝 B. 加热氧化银制银
C. CO还原铁矿石制铁 D. 电解食盐水制钠
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省南京市高二学业水平模拟测试化学试卷(解析版) 题型:选择题
水能参与很多化学反应。下列物质不能与水反应的是
A. Na B. Cl2 C. CaO D. SiO2
查看答案和解析>>
科目:高中化学 来源:2017届山东省青岛市高三第一次统一质量检测理综化学试卷(解析版) 题型:选择题
短周期主族元素,a、b、c、d的原子序数依次增大。四种元素形成的单质依次为m、n、p、q;x、y、z是这些元素组成的二元化合物,其中z为形成酸雨的主要物质之一;25℃0.01mol·L-1w溶液中,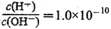 。上述物质的转化关系如图所示。下列说法正确的是
。上述物质的转化关系如图所示。下列说法正确的是
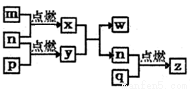
A. 原子半径的大小:a<b<c<d B. 氢化物的沸点:b>d
C. x的电子式为: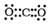 D. y、w含有的化学键类型完全相同
D. y、w含有的化学键类型完全相同
查看答案和解析>>
科目:高中化学 来源:2017届安徽省“江南十校”高三3月联考理综化学试卷(解析版) 题型:简答题
Zn(OH)2可溶于氨水生成[Zn(NH3)4]2+: Zn(OH)2+4NH3·H2O=Zn(NH3)4]2++4H2O+2OH-
(1)原子序数比Zn元素小1的元素符号为____,该元素原子基态核外电子排布式为______。
(2)NH3、H2O的沸点均高于同族元素氢化物的沸点,是因为________。
(3)NH3中N原子轨道的杂化类型是______。
(4)与H2O分子互为等电子体的分子为_____。
(5)闪锌矿是一种自然界含Zn元素的矿物,其晶体结构属于立方晶体(如右图所示),则在立方ZnS晶体结构中S2-的配位数为________。Zn2+的分数坐标为(l/4,l/4,l/4)、(3/4, 3/4,l/4)、(3/4,l/4,3/4)、(1/4,3/4,3/4),则S2-的分数坐标为______。

查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省扬州市宝应县高二下学期学业水平测试(三)化学试卷(解析版) 题型:选择题
我国首创的海洋电池以铝板、铂网为电极,以海水作为电解质溶液,电池总反应为:4Al+3O2+6H2O=4Al(OH)3,下列有关该电池说法正确的是
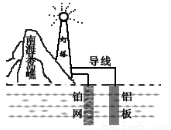
A. 该电池工作时将电能转化为化学能
B. 通常一段时间后该电池只需更换铝板就可继续使用
C. 负极反应式是:O2 + 2H2O+ 4e- = 4OH-
D. 铝片发生还原反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省哈尔滨市高二3月月考化学试卷(解析版) 题型:选择题
实验室用锌粒与VmL浓度为10%的稀硫酸反应制取氢气,若向反应混合物中加入下列物质,关于反应速率v说法正确的是
A. 少量Na2SO4固体,v(H2)减小 B. VmLBaCl2溶液,v(H2)不变
C. 加入细小的碳粒,v(H2)增大 D. 加入NH4HSO4固体,v(H2)不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com