
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列叙述中正确的是( )
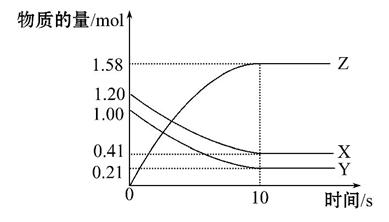
A.从反应开始到10 s时,用Z表示的反应速率为0.158 mol·L-1·s-1
B.10 s后,该反应停止进行
C.反应的化学方程式为2X(g)+Y(g)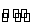 2Z(g)
2Z(g)
D.从反应开始到10 s时,平均反应速率v(X)=v(Y)=0.039 5 mol·L-1·s-1
选D。由题图可得Z表示的反应速率为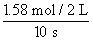 =0.079 mol·L-1·s-1,则A错误;在10 s时各组分浓度不为0,因此该反应为可逆反应,平衡时反应没有停止,为动态平衡,B错误;从反应开始到10 s时,各组分的浓度变化为Δn(X)=1.20 mol-0.41 mol=0.79 mol,Δn(Y)=1.00 mol -0.21 mol=0.79 mol,Δn(Z)=1.58 mol-0 mol=1.58 mol,由于化学计量数之比等于各组分物质的量变化之比,所以X、Y、Z的化学计量数之比为1∶1∶2,则反应的化学方程式为X(g)+Y(g)
=0.079 mol·L-1·s-1,则A错误;在10 s时各组分浓度不为0,因此该反应为可逆反应,平衡时反应没有停止,为动态平衡,B错误;从反应开始到10 s时,各组分的浓度变化为Δn(X)=1.20 mol-0.41 mol=0.79 mol,Δn(Y)=1.00 mol -0.21 mol=0.79 mol,Δn(Z)=1.58 mol-0 mol=1.58 mol,由于化学计量数之比等于各组分物质的量变化之比,所以X、Y、Z的化学计量数之比为1∶1∶2,则反应的化学方程式为X(g)+Y(g)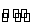 2Z(g),C错误;又由于反应速率之比等于化学计量数之比,所以从反应开始到10 s时,平均反应速率v(X)=v(Y)=
2Z(g),C错误;又由于反应速率之比等于化学计量数之比,所以从反应开始到10 s时,平均反应速率v(X)=v(Y)= (Z)=0.039 5 mol·L-1·s-1,D正确。
(Z)=0.039 5 mol·L-1·s-1,D正确。


 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
已知 X、Y、Z、Q、R、E六种元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如表.
| 元素 | 结构或性质信息 |
| X | 原子的L层上s电子数等于p电子数. |
| Y | 原子核外的L层有3个未成对电子. |
| Z | 原子的最外层电子数是次外层电子数的3倍. |
| Q | 单质常温、常压下是气体,原子的M层上有1个未成对的p电子. |
| R | 核电荷数是Y与Q的核电荷数之和. |
| E | 生产和生活中用量最大的金属. |
请根据信息回答有关问题:
(1)元素Y的核外电子排布式为 .
(2)元素X与Z可形成化合物XZ2,XZ2属于 晶体,电子式为 .
(3)X、Y、Z三种元素的电负性由高到低的排列次序依次为(写元素符号) .
(4)X、Z、Q元素均表现最低化合价时的三种氢化物中,沸点最高的是(写化学式) .
(5)R的一种配合物的化学式为RCl3•6H2O.已知0.01mol RCl3•6H2O在水溶液中用过量硝酸银溶液处理,产生0.02mol AgCl沉淀.此配合物最可能是 .
A.[R(H2O)6]Cl3 B.[R(H2O)5Cl]Cl2•H2O
C.[R(H2O)4Cl2]Cl•2H2O D.[R(H2O)3Cl3]•3H2O
(6)E能形成E2+和E3+两种价态的离子,检验E2+中含有 E3+的最佳试剂是 ,要除去E2+中E3+可加入 ,离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
在研究物质变化时,人们可以从不同的角度、不同的层面来认识物质变化时所引起的化学键及其能量变化,据此判断以下叙述中错误的是( )
A.化学反应的实质是旧化学键断裂和新化学键的形成
B.所有的化学变化一定遵循质量守恒和能量守恒
C.在化学反应中,破坏旧化学键吸收的能量大于形成新化学键释放的能量时,该反应是放热反应
D.化学键的变化必然会引起能量变化,所以能量变化也一定会引起化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
在一个密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8 mol·L-1和
5.4 mol·L-1,在一定条件下它们反应生成NH3,10 min后测得N2的浓度是
0.8 mol·L-1,则在这10 min内NH3的平均反应速率是( )
A.0.1 mol·L-1·min-1 B.0.3 mol·L-1·min-1
C.0.2 mol·L-1·min-1 D.0.6 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
胶状液氢(主要成分是H2和CH4)有希望用于未来的运载火箭和空间运输系统。实验测得:101 kPa,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量;1 mol CH4完全燃烧生成液态水和CO2,放出890.3 kJ的热量。下列热化学方程式书写正确的是( )
A.CH4(g)+2O2(g)====CO2(g)+2H2O(l) ΔH=+890.3 kJ·mol-1
B.CH4(g)+2O2(g)====CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
C.CH4(g)+2O2(g)====CO2(g)+2H2O(l) ΔH=-890.3 kJ
D.2H2(g)+O2(g)====2H2O(l) ΔH=-571.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,不属于四种基本反应类型是( )
|
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | 2HClO═2HCl+O2↑ |
|
| C. | Fe+2FeCl3═3FeCl2 | D. | CuO+CO |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
|
| A. | 铁与稀硫酸反应:2Fe+6H+=2Fe3﹢+3H2↑ |
|
| B. | Al(OH)3沉淀中滴加盐酸:Al(OH)3+H﹢=Al3﹢+H2O |
|
| C. | 碳酸氢钠溶液中加入氢氧化钠:HCO3﹣+OH﹣=CO32﹣+H2O |
|
| D. | 碳酸钙与稀硝酸反应:CO32﹣+2H+=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
配制500mL 0.5mol•L﹣1的NaOH溶液,试回答下列问题:
(1)计算:需要NaOH固体的质量为 g .
(2)某学生用托盘天平称量一个小烧杯的质量,称量前把游码放的标尺的零刻度处,天平静止时发现指针在分度盘的偏右位置,此时左边的托盘将 (填“高于”或“低于”)右边的托盘,欲使天平平衡,所进行的操作为 .假定最终称得小烧杯的质量为 (填“32.6g”或“32.61 g”).
(3)配制方法:设计五个操作步骤
①向盛有NaOH的烧杯中加入200 mL 蒸馏水使其溶解,并冷却至室温.
②继续往容量瓶中加蒸馏水至液面接近刻度线1 cm~2 cm.
③将NaOH溶液沿玻璃棒注入500 mL容量瓶中
④在烧杯中加入少量的蒸馏水,小心洗涤2~3次后移入容量瓶
⑤改用胶头滴管加蒸馏水至刻度线,加盖摇匀.
试将以上操作按正确顺序编出序号 .
(4)某学生实际配制NaOH溶液的浓度0.48mol•L﹣1,原因可能是
A. 使用滤纸称量氢氧化钠固体 B. 容量瓶中原来存有少量蒸馏水
C. 溶解后的烧杯未经多次洗涤 D.定容时仰视刻度.
查看答案和解析>>
科目:高中化学 来源: 题型:
锌锰电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s),下列说法错误的是( )
|
| A. | 电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
|
| B. | 电池负极的电极反应式为Zn﹣2e﹣+2 OH﹣=Zn(OH)2 |
|
| C. | 电池工作时,电流由正极通过外电路流向负极 |
|
| D. | 碱性锌锰电池是二次电池 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com