
����Ŀ��ʵ�������屽������ͼװ�á���ش���������:
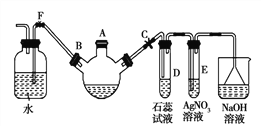
��1���ر�F��,��C��,��װ����������������ƿ��A�ڼ�������,�ټ�������м,��סA��,��������ƿ�з������л���ѧ��Ӧ����ʽΪ____��
��2��D�Թ��ڳ��ֵ�����Ϊ______;E�Թ��ڳ��ֵ�����Ϊ______��
��3����������ƿ����������ð��ʱ��F��,�ر�C��,�ɿ�����������__________��
��4�����屽�г�ȥ��,��NaOH��Һ��������ϴ��,��Ӧ�����ӷ���ʽΪ_________��
��5���ұ��ļ���ԭ�ӿ����ڹ��������º�Cl2����ȡ����Ӧ����д���õ�ȡ���������ȥ��Ӧ�Ļ�ѧ����ʽ_____________��
���𰸡� ![]() +Br2
+Br2![]()
![]() +HBr �а�������,��Һ��� ����dz��ɫ���� Һ�嵹�� , ������ƿ��Һ��ֲ� Br2 + 2OH-
+HBr �а�������,��Һ��� ����dz��ɫ���� Һ�嵹�� , ������ƿ��Һ��ֲ� Br2 + 2OH-![]() Br- + BrO- + H2O
Br- + BrO- + H2O 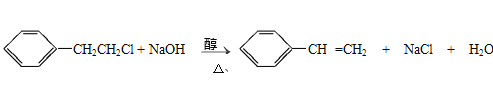
����������1����������ƿ�������������廯�������������廯��������������������ȡ����Ӧ�����屽���廯�⣬���Է�����Ӧ�Ļ�ѧ����ʽΪ![]() +Br2
+Br2![]()
![]() +HBr����2�����������廯��������������������ȡ����Ӧ�����屽���廯�⣬�廯���ӷ������ԣ����Թ�D�п���������Ϊ�а�����������Һ��죻�廯������ˮ����������Ӧ�����廯��dz��ɫ���������Թ�E������Ϊ������dz��ɫ��������3�������廯�⼫������ˮ�����Դ�������ƿ�еķ�Ӧ���е���������ð��ʱ��F�У��ر�C�У����Կ�������������B�����Ĺ��ƿ��ˮ������������ƿ���屽������ˮ������������ƿ�л���ֲַ㣻��4��������ƿ�е��屽�к����������壬������NaOH��Һ��ȥ����Ӧ���ӷ���ʽΪBr2+2OH-��Br-+BrO-+H2O����5���ұ��ļ���ԭ�ӿ����ڹ��������º�Cl2����ȡ����Ӧ���õ�ȡ��������
+HBr����2�����������廯��������������������ȡ����Ӧ�����屽���廯�⣬�廯���ӷ������ԣ����Թ�D�п���������Ϊ�а�����������Һ��죻�廯������ˮ����������Ӧ�����廯��dz��ɫ���������Թ�E������Ϊ������dz��ɫ��������3�������廯�⼫������ˮ�����Դ�������ƿ�еķ�Ӧ���е���������ð��ʱ��F�У��ر�C�У����Կ�������������B�����Ĺ��ƿ��ˮ������������ƿ���屽������ˮ������������ƿ�л���ֲַ㣻��4��������ƿ�е��屽�к����������壬������NaOH��Һ��ȥ����Ӧ���ӷ���ʽΪBr2+2OH-��Br-+BrO-+H2O����5���ұ��ļ���ԭ�ӿ����ڹ��������º�Cl2����ȡ����Ӧ���õ�ȡ��������![]() ��������ȥ��Ӧ�Ļ�ѧ����ʽΪ
��������ȥ��Ӧ�Ļ�ѧ����ʽΪ![]() ��
��


 �γ̴����Ծ�����100��ϵ�д�
�γ̴����Ծ�����100��ϵ�д� �¾�����ĩ���100��ϵ�д�
�¾�����ĩ���100��ϵ�д� ȫ�ܴ���100��ϵ�д�
ȫ�ܴ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����b L Al2(SO4)3��(NH4)2SO4�Ļ����Һ�м���a mol BaCl2��ǡ��ʹ��Һ�е�SO42-��������ȫ���������������ǿ����ȿɵõ�c mol NH3����ԭ��Һ�е�Al3+Ũ�ȣ�mol/L��Ϊ
A. (2a-c)/b B. (2a-c)/2b C. (2a-c)/3b D. (2a-c)/6b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��A��B��C��D,ԭ��������������A�Ļ�̬ԭ�ӵ�L�������K����ӵ�������B�ļ۵��Ӳ��е�δ�ɶԵ�����3����C��Bͬ����D����ۺ�����Ϊ������ǿ���������ᡣ��ش��������⣺
��1��C�Ļ�̬ԭ�ӵĵ����Ų�ʽΪ___________��D����ۺ��������Ա�������۵ĺ���������ǿ��ԭ����_____________________________________________��
��2���ӻ������Ϊ���ԺͲ������ӻ����������ӻ�ʱ���ӻ�������в��μӳɼ��ŵ��ӶԵĴ��ڡ�A��B��C���ֱ�����D�γ�����ԭ���ӻ���ʽ��Ϊ___________�Ĺ��ۻ�����X��Y��Z�����У����ڲ������ӻ�����___________ (д��ѧʽ)��
��3���Ƚ�Y��Z���۷е�Y______Z(����>������<������=��)������������_____________________��
��4��DԪ������Cu�γ��ػ�ɫ���壬��ˮ�ܽⲢϡ�����У���Һ��ɫ����ɫ��ת��Ϊ��ɫ������ɫ������_________________������ɫ�����е���λԭ��________________��
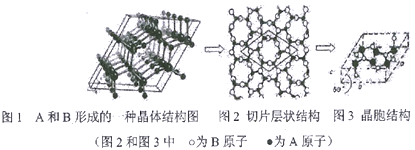
��5��A��B���γɶ��ֽṹ�ľ��塣����һ������ʯī�Ľṹ����ṹ����ͼ��ʾ(ͼ1Ϊ����ṹ��ͼ2Ϊ��Ƭ��״�ṹ)���仯ѧʽΪ__________��ʵ���ô˾���ṹ����������ϵ,�����ṹ��ͼ3����֪ͼʾԭ�Ӷ������ھ����ڣ���������a=0.64nm��c=0.24nm���侧���ܶ�Ϊ__________g/cm3(��֪��2=1.414,��=1.732,�����ȷ��С������2λ��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
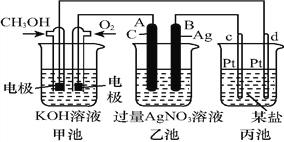
����Ŀ����ͼ��һ����ѧ���̵�ʾ��ͼ:
��ش�:
��1��ͼ�м׳���______װ�ã�����OH������_________��(����CH3OH������O2��)��
��2��д��ͨ��CH3OH�缫�ĵ缫��Ӧʽ:_______________________________��
��3�����ҳ����缫�����μ�������ɫʯ����Һ���������ĵ缫Ϊ_____��(����A������B��)��
��д���˵缫�ĵ缫��Ӧʽ:______________________��
��4���ҳ��з�Ӧ�����ӷ���ʽΪ________________________��
��5�����ҳ���B(Ag)����������5.40 gʱ���ҳ�c(H+)��_______(���ҳ�����ҺΪ500 mL)����ʱ����ij�缫����1.60 gij����������е�ij����Һ������_________(�����)��
A��MgSO4 B��CuSO4 C��NaCl D��AgNO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֤�������������ʵ����ʵ��
A. CH3COOH��Һ��Zn��Ӧ�ų�H2
B. 0.1 mol��L��1 CH3COONa��Һ��pH����7
C. CH3COOH��Һ��Na2CO3��Ӧ����CO2
D. 0.1 mol��L��1 CH3COOH��Һ��ʹ��ɫʯ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�pH�仯���ж��У���ȷ������ ��
A. ���¶ȵ����ߣ���ˮ��Kw��С
B. ���¶ȵ����ߣ���ˮ��pH����
C. ������ˮ������һ��ʱ���pH��С
D. ����������Һ�����ڿ����У�pH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijУѧ������С���ͬѧ�����ͼ��ʾʵ��װ�ã�������֤һ����̼���л�ԭ�ԡ���֪��ʯ�ҵijɷ����������ƺ������ƵĻ���̿��ˮ�����ڸ��������·������·�Ӧ��C + H2O��g��![]() CO + H2���ش��������⣺
CO + H2���ش��������⣺
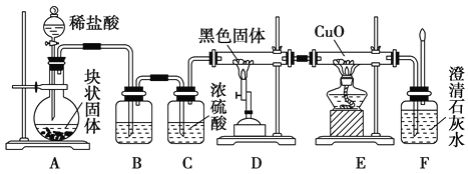
(1)д��װ��A�з�����Ӧ�����ӷ���ʽ____________________��
(2)��ʵ����û��װ��C��ʹװ��B��װ��Dֱ�����������ʵ����ɵ�Ӱ���ǣ�____________��
(3)װ��D�к�ɫ����Ϊ___________ (������)��
(4)������ͼװ�ý���ʵ��ʱ�����Ƚ��еIJ�����___________________________________ ��
(5)����ʵ���е�____________________________����֤��CO���л�ԭ�ԡ�
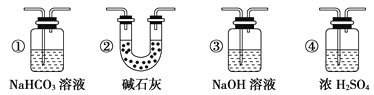
(6)��Ҫ����װ��F�г���ʯ��ˮ����ǵ�����ȷ��һ����̼���л�ԭ�ԣ�Ӧ����ͼװ��____��____֮��������ͼ�е�____________________װ��(�����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���ܱ��������м���һ�����ɻ����ĸ���(��Ȳ���)�������ֳ������֣�����߳���8molN2,�ұ߳���CO��CO2�Ļ�����干64g ʱ�����崦����ͼλ��(�����¶Ȳ���),����˵����ȷ����

A. �ұ�CO��CO2������֮��Ϊ1:3
B. �Ҳ�CO������Ϊ14g
C. �Ҳ������ܶ�����ͬ�����������ܶȵ�2��
D. ���ı��ұ�CO��CO2�ij�������ʹ���崦�ھ����Ҷ�1/3���������¶Ȳ��䣬��ǰ�����γ�����������ڵ�ѹǿ֮��Ϊ5: 6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ѧ��ѧ�г����ڻ����ķ�����ᴿ��װ�ã������װ�ûش����⣺

��1�����Ȼ�����Һ�еõ��Ȼ��ع��壬ѡ��װ��________(�����װ��ͼ����ĸ����ͬ)����ȥ����ˮ�е�Cl�������ʣ�ѡ��װ��________��
��2������ˮ������з����ֲ���ͣ�ѡ��װ��________���÷��뷽��������Ϊ________��
��3��װ��A�Тٵ�������________����ˮ�ķ����Ǵ�________����ϡ����¡����ڽ�ˮ��װ��B�ڷ�Һʱ�ϲ�Һ���________�����������ƣ���________����ϡ����¡�����������
��4����ˮ���̲��ŷḻ����Դ����ʵ������ȡ������ˮ�������������̵�ʵ�飺
![]()
![]()
![]()
![]()
![]() �D��
�D��![]()
�����к�Ca2����Mg2����Fe3����![]() �����ʣ���Ҫ�ᴿ������ۺ����á������ᴿ�IJ����У�
�����ʣ���Ҫ�ᴿ������ۺ����á������ᴿ�IJ����У�
�ټ��������Na2CO3��Һ���ڼ��������BaCl2��Һ���ۼ��������NaOH��Һ���ܵ�����Һ��pH����7�����ܽ⡡���ˡ�������
��ȷ�IJ���˳����________(��ѡ����ĸ)��
a���ݢڢۢ٢ޢܢ� b���ݢ٢ڢۢޢܢ�
c���ݢڢ٢ۢܢޢ� d���ݢۢڢ٢ޢܢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com