
某实验小组欲探究碳与浓硝酸反应的情况。甲同学设计了图1装置,认为若有红棕色气体产生就说明碳与浓硝酸发生了反应。
(1)乙同学认为甲同学的结论是错误的,他的理由是 (用化学方程式表示),所以他认为应该检验 (填化学式)的产生来证明碳与浓硝酸反应。为此乙同学查阅相关资料得知“0℃时四氧化二氮为液体”,从而改进了实验装置如图2所示。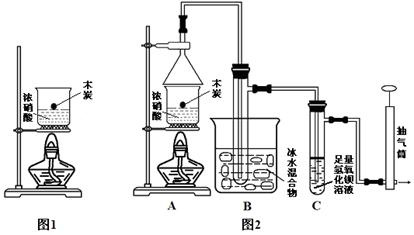
(2)为了减少干扰,对于A装置有下面4种操作方案,其中最合理的是(填写数字序号) 。
①将炭与浓硝酸一同放在装置中加热;②先加热浓硝酸,然后将炭投入其中;
③先加热炭,再加入冷浓硝酸; ④先加热炭,再将炭投入冷浓硝酸。
(3)请用平衡移动原理解释B装置的作用 。
(4)C装置中出现的现象是 ,经检测C的溶液中还含有少量氮元素,只以NO3-形式存在,写出生成该离子的化学方程式 。
(1)4HNO3 4NO2↑+O2↑+2H2O(2分) CO2(1分)
4NO2↑+O2↑+2H2O(2分) CO2(1分)
(2)④(2分)
(3)常温下存在平衡体系:2NO2 N2O4,降低温度N2O4液化,平衡右移,除去混合气体中的NO2。(3分)
N2O4,降低温度N2O4液化,平衡右移,除去混合气体中的NO2。(3分)
(4)C中溶液变浑浊(或产生白色沉淀) (3分) 4NO2+O2+2Ba(OH)2=2Ba(NO3)2+2H2O(3分)
解析试题分析:(1)浓硝酸受热易分解产生二氧化氮气体,4HNO3 4NO2↑+O2↑+2H2O;若C与浓硝酸反应应有二氧化碳气体生成,所以检验CO2的产生来证明碳与浓硝酸反应;
4NO2↑+O2↑+2H2O;若C与浓硝酸反应应有二氧化碳气体生成,所以检验CO2的产生来证明碳与浓硝酸反应;
(2)只要存在浓硝酸被加热的情况都有可能产生二氧化氮气体,不能证明是C与浓硝酸发生了反应,所以最合理的操作是④;
(3)常温下存在平衡体系:2NO2 N2O4,该反应为放热反应,所以降低温度,平衡正向移动,N2O4被液化,从而除去NO2;
N2O4,该反应为放热反应,所以降低温度,平衡正向移动,N2O4被液化,从而除去NO2;
(4)若C与浓硝酸反应则有二氧化碳生成,与氢氧化钡溶液反应生成白色沉淀;C的溶液中还含有少量氮元素,只以NO3-形式存在,说明混合气体中仍有NO2,与氢氧化钡溶液、氧气反应生成硝酸钡溶液,化学方程式为4NO2+O2+2Ba(OH)2=2Ba(NO3)2+2H2O。
考点:考查对实验的分析判断能力,平衡理论的应用,化学方程式的书写


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:计算题
(本题共14分)
硫有多种含氧酸,亚硫酸(H2SO3)、硫酸(H2SO4)、焦硫酸(H2SO4·SO3)、硫代硫酸(H2S2O3)等等,其中硫酸最为重要,在工业上有广泛的应用。在实验室,浓硫酸是常用的干燥剂。
完成下列计算:
(1)焦硫酸(H2SO4·SO3)溶于水,其中的SO3都转化为硫酸。若将445g焦硫酸溶于水配成4.00L硫酸,该硫酸的物质的量浓度为________mol/。
(2)若以浓硫酸吸水后生成的H2SO4·H2O计算,250g质量分数为98%的硫酸能吸收多少g水?
(3)硫铁矿是工业上制硫酸的主要原料。硫铁矿氧化焙烧的化学反应如下:
3FeS2+8O2→Fe3O4+6SO2 4FeS2+11 O2→2Fe2O3+8SO2
若48mol FeS2完全反应耗用氧气2934.4L(标准状况),计算反应产物中Fe3O4与Fe2O3物质的量之比。
(4)用硫化氢制取硫酸,既能充分利用资源又能保护环境,是一种很有发展前途的制备硫酸的方法。
硫化氢体积分数为0.84的混合气体(H2S、H2O、N2)在空气中完全燃烧,若空气过量77%,计算产物气体中SO2体积分数(水是气体)。(已知空气组成:N2体积分数0.79、O2体积分数0.21)
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(16分)氯气可与潮湿的消石灰反应制取少量漂白粉,也可在浓溶液条件下与石灰石反应生成较浓的HClO溶液。
Ⅰ.甲研究性学习小组利用氯气制少量漂白粉(如图所示):
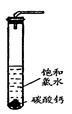
(1)A仪器的名称是 ,所盛试剂是 。
(2)此实验结果所得Ca(ClO)2产率太低。经分析并查阅资料发现主要原因是在U型管中存在两个副反应:
①温度较高时氯气与消石灰反应生成了Ca(ClO3)2,为避免此副反应的发生,可采取的措施是 。此副反应的化学方程式为: 。
②写出另一个副反应的化学方程式 。为避免此副反应发生,可在BC之间加多一个装置,请在答题卷的方框中画出该装置,并标明所用的试剂。
Ⅱ. 乙研究性学习小组研究饱和氯水与石灰石的反应:
①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水(如图所示),充分反应,有少量气泡产生,溶液浅黄绿色褪去;
②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生。 经检测,上述实验中产生的无色气体均为CO2。请回答:
(3)反应后所得的溶液漂白性增强的原因是 。
(4)依据上述实验可推知:②的滤液中的溶质除CaCl2、HClO外,还含有 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
硫化碱法是工业上制备Na2S2O3的方法之一,反应原理为:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2(该反应△H>0)。某研究小组在实验室用硫化碱法制备Na2S2O3·5H2O流程如下。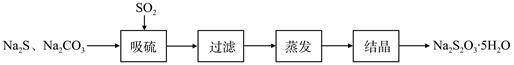
(1)吸硫装置如图所示。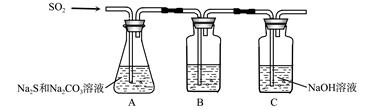
①装置B的作用是检验装置A中SO2的吸收效率,B中试剂是 ,表明SO2吸收效率低的实验现象是B中溶液 。
②为了使SO2尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是 、 。(写出两条)
(2)假设本实验所用的Na2CO3含少量NaCl、NaOH,设计实验方案进行检验。(室温时CaCO3饱和溶液的pH=10.2)
限选试剂及仪器:稀硝酸、AgNO3溶液、CaCl2溶液、Ca(NO3)2溶液、酚酞溶液、蒸馏水、pH计、烧杯、试管、滴管
| 序号 | 实验操作 | 预期现象 | 结论 |
| ① | 取少量样品于试管中,加入适量蒸馏水,充分振荡溶解,___________________。 | _______________ | 样品含NaCl |
| ② | 另取少量样品于烧杯中,加入适量蒸馏水,充分搅拌溶解,___________________。 | _______________ | 样品含NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
安徽省从2013年12月1日零时起,车用汽油升级为“国Ⅳ”标准,对二氧化硫的排放有了大大的改善。已知SO2可以用Fe( NO3)3溶液吸收, 0.1mol/L的Fe(NO3)3溶液的pH=2。某学习小组据此展开如下相关探究:
【探究I】铜与浓硫酸的反应探究:
(l)取12.8g铜片于三颈烧瓶中,通N2一段时间后再加入20 mL 18 mol?L-1的浓硫酸,加热。装置A中有白雾(硫酸酸雾)生成,装置B中产生白色沉淀,充分反应后,烧瓶中仍有铜片剩余。
①该小组同学认为烧瓶中除有铜片剩余外还应有较多的硫酸剩余,其原因是: ___________________ 。
②该小组同学欲通过测定产生气体的量来求余酸的物质的量,设计了多种实验方案。下列方案不可行的是______ 。
A.将产生的气体缓缓通过预先称量的盛有碱石灰的干燥管,结束反应后再次称重
B.将产生的气体缓缓通入足量硫酸酸化的高锰酸钾溶液后,再加入足量的BaCl2溶液,测量所得沉淀的质量
C.用排饱和NaHSO3溶液的方法测定其产生气体的体积(折算成标准状况)
【探究II】装置B中产生沉淀的原因探究:
(2)加入浓硫酸之前先通N2一段时间,其目的是____ 。
(3)经过讨论,该小组对装置B中产生沉淀的原因,提出下列猜想(不考虑各因素的叠加):
猜想1: 装置A中的白雾进入B参与反应
猜想2:SO2被Fe3+氧化为SO42-
猜想3: 。
(4)甲同学认为只要在装置A、B间增加洗气瓶C,就可以排除装置A中白雾影响,则C中盛放的试剂是 。
(5)乙同学取出少量装置B中清液,加入几滴酸性高锰酸钾,发现紫红色褪去,据此认为猜想2成立。你是否同意其结论?并说明理由: 。
【思考与交流】
(6)实验结束后,若使烧瓶中铜片继续溶解,下列方案(必要时可加热)可行的是 。
A.打开弹簧夹,通入O2 B.由分液漏斗加入H2O2溶液
C.由分液漏斗加入NaNO3溶液 D.由分液漏斗加入Na2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
氨水是一种的常用的化学试剂。
(1)以浓氨水和生石灰为原料,用如下装置为发生装置,可制取少 量氨气。已知:NH3·H2O+CaO=Ca(OH)2+NH3↑。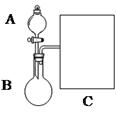
①生石灰应该装在 (填A或B)。
②试从电离平衡角度分析该实验中氨气逸出的原因: 。
③现要用试管和必要实验用品收集一试管氨气,请在C处补充相应收集装置。
(2)化学兴趣小组用氨水与硝酸银溶液配制好银氨溶液后,进行乙醛的银镜反应实验,但部分同学实验时间长,且效果不明显。影响乙醛银镜反应速率的因素有哪些呢?请你完成如下猜想:
①猜想:因素一:银氨溶液的pH大小;
因素二: 。
②你设计实验验证上述影响因素一,完成下表中内容。
提供试剂:乙醛、2%稀氨水、 0.25mol/L NaOH溶液、盐酸 、 2% AgNO3溶液
实验用品:烧杯(装有热水)、试管
| 实验步骤 | 实验操作 | 预期现象及结论(步骤1只填现象) |
| 1 | 在A、B两支洁净的试管中各入1mL 2%的AgNO3溶液,然后边振荡试管边逐滴滴入2%稀氨水,至最初产生的沉淀恰好完全溶解,此时制得pH均约为8的银氨溶液。 | |
| 2 | | |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
新制氯水中含有多种粒子,某校化学研究性学习小组的同学为探究其性质,做了如下实验,请你帮助完成:
(1)HClO不稳定,见光易分解生成HCl和O2。请设计实验证明有O2生成 。
(2)氯气能使湿润的红色布条退色。对于使湿润的红色布条退色的物质,同学们的看法不一致,认为氯水中存在的几种粒子都有可能。请你设计实验,得出正确结论。
| 提出问题 | 收集资料 | 提出假设 | 验证假设 | 得结论出 |
| 氯水中何种物质能使湿润的红色布条退色? | ①氯气有强氧化性 ②氯气与冷水反应生成盐酸和次氯酸 ③次氯酸有强氧化性 | ① ② ③ ④H2O使布条退色 | ①:实验①:把红色干布条放入充满氯气的集气瓶中,布条不退色 实实验②: ; 实验③:把红色布条放在水里,布条不退色 | |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某校化学实验兴趣小组为了验证在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),请按要求回答下列问题。
(1)下列方法中,可制得Cl2的正确组合是 。
①MnO2和浓盐酸混合共热;②MnO2、NaCl和浓硫酸混合共热;③NaClO和浓盐酸混合;④K2Cr2O7和浓盐酸混合;⑤KClO3和浓盐酸混合共热;⑥KMnO4和浓盐酸混合。
A.①②⑥ B.②④⑥
C.①④⑥ D.全部可以
(2)写出实验室制取Cl2的离子方程式 。
(3)①装置B的作用是 ;
②装置C和D出现的不同现象说明的问题是 ;
③装置E的作用是 。
(4)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出应该在装置 与 之间(填装置字母序号)增加一个装置,所增加装置里面的试剂可以为 (填字母序号)。
A.湿润的碘化钾淀粉试纸 B.浓硫酸
C.湿润的红色布条 D.饱和食盐水。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
实验室用铜制取硫酸铜,将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体。
(1)为了节约原料,硫酸和硝酸的最佳物质的量之比为________ ;为了吸收该反应中产生的尾气,可选择的最佳装置是________(填序号)。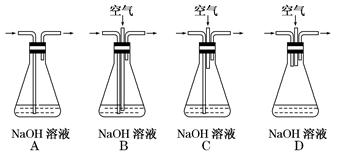
(2)为符合绿色化学的要求,某研究性学习小组进行如下设计。
方案1:以空气为氧化剂。将铜粉在仪器N中反复灼烧,使铜与空气充分反应生成氧化铜,再使氧化铜与稀硫酸反应。
方案2:将空气或氧气直接通入到铜粉与烯硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4,再通入空气或氧气,即发生反应,生成硫酸铜。反应完全后,加入物质甲调节pH,铁元素全部转化为Fe(OH)3沉淀(一般当铁离子的浓度下降到10-5mol·L-1时,就认为沉淀完全),然后过滤、浓缩、结晶。
(已知:常温下,Ksp[Cu(OH)2]=10-22,Ksp[Fe(OH)3]=10-38)
请回答下列问题:
①方案1中仪器N的名称是________。
②方案2中为了使铁元素全部沉淀,应调节pH至少为________。
③方案2中甲物质可选用________(填序号)。
| A.CaO | B.NaOH | C.CuCO3 | D.Cu2(OH)2CO3 E.Fe2(SO4)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com