

| 污 染 指 数 | 首要 污染物 | 空气 质量等级 | ||
| SO2 | NO2 | PM10 | ||
| 23 | 35 | 56 | PM10 | 良 |
分析 (1)PM10是指空气中直径等于和小于10微米的颗粒物;
(2)依据各项污染物污染指数分别为:SO2-58,NO2-21,PM10-23及空气污染指数(API)与空气质量等级关系判断解答;
(3)依据酸雨的概念及引起酸雨物质的性质解答;
(4)依据S+O2═SO2,计算生成二氧化硫的物质的量及标况下体积;治理酸雨的措施从减少二氧化硫排放角度解答.
解答 解:(1)PM10是指空气中直径等于和小于10微米的可吸入颗粒物;
故答案为:可吸入颗粒物;
(2)依据各项污染物污染指数分别为:SO2-58,NO2-21,PM10-23及空气污染指数(API)与空气质量等级关系,可知二氧化硫指数超标为当日首要污染物;58+21+23=102,空气质量级别为 良;
故答案为:二氧化硫(SO2); 良;
(3)酸雨为pH值小于5.6的雨水,形成酸雨的主要原因为二氧化硫与氮的氧化物的排放,二氧化硫溶于水与水反应生成亚硫酸,亚硫酸为弱酸显酸性,且亚硫酸不稳定容易被氧化为硫酸,硫酸为强酸,所以随着时间的推移,pH变小;
故答案为:<;变小;
(4)依据方程式得:
S+O2 ═SO2,
32g 22.4L
1OOO×0.032%×103 V 解得V=22.4L;
治理酸雨的措施应减少二氧化硫的排放,如:使用清洁能源、燃煤脱硫等;
故答案为:22.4 使用清洁能源、燃煤脱硫等.
点评 本题考查环境污染及治理,为高频考点,有利于培养学生良好的科学素养,提高学习的积极性,难度不大,注意相关基础知识的积累.


科目:高中化学 来源: 题型:解答题
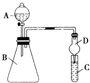 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验:
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 自然界里没有任何一种食物能同时满足人体对各种维生素的需要 | |
| B. | 用于2008年北京奥运“祥云”火炬的丙烷是一种清洁燃料 | |
| C. | 用大米酿的酒在一定条件下密封保存,时间越长越香醇 | |
| D. | 葡萄糖、蔗糖、纤维素和脂肪在一定条件下都可以发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaNO2是还原剂 | |
| B. | NH4Cl中N元素被还原 | |
| C. | 生成1 mol N2时转移6 mol电子 | |
| D. | 氧化剂和还原剂的物质的量之比是1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 64 g•mol-1 | B. | 24 g•mol-1 | C. | 56 g•mol-1 | D. | 188 g•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com