
【题目】根据题意解答
(1)某实验小组同学进行如下实验,以检验化学反应中的能量变化,实验中发现,反应后①中的温度升高;②中的温度降低.由此判断铝条与盐酸的反应是热反应,Ba(OH)28H2O与NH4Cl的反应是热反应.反应过程(填“①”或“②”)的能量变化可用图2表示. 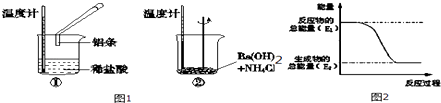
(2)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的是(填序号). 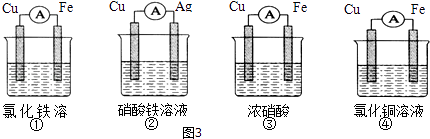
(3)将CH4设计成燃料电池,其利用率更高,装置如图4所示(a、b为多孔碳棒).处电极入口通甲烷(填A或B),其电极反应式为 . 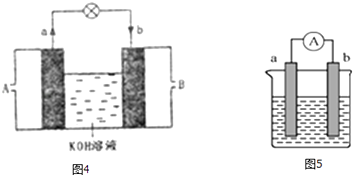
(4)如图5是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题: ①当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,写出该原电池正极的电极反应式为 .
②当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该原电池的正极为;该原电池的负极反应式为 .
【答案】
(1)放;吸;①
(2)②
(3)A;CH4﹣8e﹣+10OH﹣=CO32﹣+7H2O
(4)2H++2e﹣═H2↑;Mg;Al+4OH﹣﹣3e﹣=AlO2﹣+2H2O
【解析】解:(1)通过实验测出,反应前后①烧杯中的温度升高,则Al跟盐酸的反应是放热反应,②烧杯中的温度降低,则Ba(OH)28H2O跟NH4Cl的反应是吸热反应;根据图2数据可知,该反应中,反应物总能量大于生成物总能量,则该反应为放热反应,可表示反应①的能量变化,所以答案是:放;吸;①;(2)验证Fe3+与Cu2+氧化性强弱,在原电池中,铜作负极、其它导电的金属或非金属作正极,电解质溶液为可溶性的铁盐,①中铁作负极、Cu作正极,电池反应式为Fe+2Fe3+=3Fe2+ , 不能验证Fe3+与Cu2+氧化性强弱,故错误;②中铜作负极、银作正极,电池反应式为Cu+2Fe3+=Cu2++2Fe2+ , 能验证Fe3+与Cu2+氧化性强弱,故正确;③中铁发生钝化现象,Cu作负极、铁作正极,电池反应式为:Cu+2NO3﹣+4H+=Cu2++2NO2↑+2H2O,不能验证Fe3+与Cu2+氧化性强弱,故错误;④中铁作负极、铜作正极,电池反应式为:Fe+Cu2+=Cu+Fe2+ , 不能验证Fe3+与Cu2+氧化性强弱,故错误;所以答案是:②;(3)根据电子流向知,A为负极、B为正极,燃料电池中通入燃料的电极为负极、通入氧化剂的电极为正极,所以A处通入甲烷,甲烷失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为CH4﹣8e﹣+10OH﹣═CO32﹣+7H2O,所以答案是:A;CH4﹣8e﹣+10OH﹣═CO32﹣+7H2O(4)①Al、Cu、稀硫酸构成的原电池,金属Al作负极,金属Cu为正极,正极上氢离子得到电子,负极上Al失去电子,正极反应为2H++2e﹣=H2↑,所以答案是:2H++2e﹣=H2↑; ②Al、Mg、NaOH溶液可构成原电池,Al为负极,Mg为正极,负极上Al失去电子,正极上水中的氢离子得到电子,发生电池离子反应为2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑,所以答案是:Mg; Al+4OH﹣﹣3e﹣=AlO2﹣+2H2O.
【考点精析】解答此题的关键在于理解反应热和焓变的相关知识,掌握在化学反应中放出或吸收的热量,通常叫反应热.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
【题目】下列叙述中一定正确的是
A.任何浓度溶液的酸碱性都可用pH试纸测定
B.某温度下,pH=6.2的纯水显酸性
C.25℃时,pH=1的醋酸溶液中c(H+)是pH=2的盐酸溶液中c(H+)的10倍
D.25℃时,pH=12的NaOH溶液中的n(OH-)=10-2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于二氧化硫的说法不正确的是( )
A. 能使某些有色物质褪色B. 无色、有刺激性气味、无毒
C. 既有氧化性、又有还原性D. 既可溶于水、又可与水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解NaCl溶液的装置如图所示,下列说法不正确的是( ) 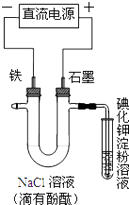
A.铁电极上的电极反应式为Fe﹣2e﹣=Fe2+
B.溶液中Na+向铁电极方向移动
C.通电一段时间后,可看到铁电极附近溶液变红
D.通电一段时间后,可看到试管中溶液变蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在阿富汗战争和伊拉克战争中美军士兵佩带的头盔、防弹背心和刚性前后防护板能够有效防御子弹和炮弹碎片,它们在战争中保住了许多美军士兵的生命.新型纤维不久将有望取代使用了数十年的凯夫拉纤维,成为未来防弹装备的主要制造材料.M5纤维是近年来开发出的一种超高性能纤维,它比现有的防爆破材料轻35%,下面是M5纤维的合成路线(部分反应未注明条件): 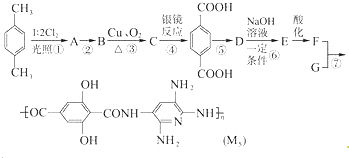
已知:当反应条件为光照且与X2反应时,通常是X2与烷或苯环侧链烃基上的H原子发生的取代反应,而当反应条件为催化剂存在且与X2反应时,通常为苯环上的H原子直接被取代.根据上述合成M5纤维的过程,回答下列问题:
(1)合成M5的单体G的结构简式为 , F的含氧官能团的名称有 .
(2)在①~⑦的反应中,不属于取代反应的是 , ②的反应条件是 .
(3)生成A的同时可能生成的A的同分异构体为 .
(4)1mol的C和足量新制的氢氧化铜悬浊液反应可以生成mol砖红色沉淀.
(5)1mol的F和Na2CO3溶液反应最多消耗Na2CO3mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学上常用燃烧法确定有机物的组成,如下图所示装置是用燃烧法确定烃或烃的含氧衍生物分子式的常用装置,这种方法是在电炉加热时用纯氧氧化管内样品,根据产物的质量确定有机物的组成. 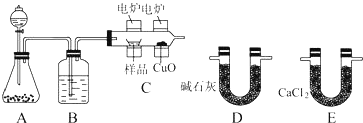
完成下列问题:
(1)A中发生反应的化学方程式为 .
(2)B装置的作用是 , 燃烧管C中CuO的作用是
(3)产生氧气按从左向右流向,燃烧管C与装置D、E的连接顺序是:C→→ .
(4)反应结束后,从A装置锥形瓶内的剩余物质中分离出固体,需要进行的实验操作是 .
(5)准确称取 1.8g 烃的含氧衍生物X的样品,经充分燃烧后,D管质量增加 2.64g,E管质量增加 1.08g,则该有机物的实验式是 . 实验测得X的蒸气密度是同温同压下氢气密度的45倍,则X的分子式为 , 1mol X分别与足量Na、NaHCO3反应放出的气体在相同条件下的体积比为1:1,X可能的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、M都是中学教材中的常见元素,(甲) XO3n﹣+Xn﹣+H+→X(单质)+H2O(未配平); (乙)Mm++mOH﹣=M(OH)m↓.下列对两个离子反应通式的推断中,正确的是( ) ①若n=1,则XO3n﹣中X元素为+5价,X位于周期表第ⅤA族
②若n=2,则X最高价氧化物的水化物可能与它的氢化物反应
③若m=1,则M(NO3)m溶液和氨水互滴时的现象可能不同
④若m=2,则在空气中蒸干、灼烧MSO4溶液一定能得到MSO4
⑤若m=3,则MCl3与足量氢氧化钠溶液反应一定生成M(OH)m .
A.①③④
B.②③
C.①②③
D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用如图所示装置制取氯水并进行相关实验.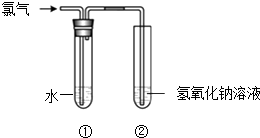
(1)装置②中反应的化学方程式是 . 装置②中的NaOH溶液换成下列也可以起到尾气处理的作用(填字母).a.NaCl溶液 b.FeSO4溶液 c.Na2SO3溶液
(2)实验进行一段时间后,装置①中溶液呈黄绿色,由此说明该溶液中一定含有的物质是(填化学式).
(3)取少量装置①中的溶液滴在蓝色石蕊试纸上,试纸先变红后褪色,说明氯水具有性.
(4)已知将氯气通入热的氢氧化钠溶液中,可发生如下反应:Cl2+NaOH→A+NaClO3+H2O(未配平)其中,A的化学式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期A,B,C,D,E,F,G原子序数依次增大,A元素的质子数和质量数相等,B元素具有三个能级且所排电子数相同,D元素2p能级上电子数是2s能级的两倍;D和E相邻且同主族.F是第四周期未成对电子最多的原子,G是目前使用量最多的金属 请回答下列问题:(用推出的元素符号或者化学式作答)
(1)F的价电子排布式为 , B,C,D三种元素的第一电离能从大到小的顺序为 .
(2)BD32﹣中B原子的杂化方式为 , 该离子的空间构型为
(3)写出一种由A,C,D组成且既含离子键又含共价键的物质的化学式 , 化合物ABC中σ键和π键数目之比为 , C的气态氢化物在一定的压强下,测得的密度比该压强下理论密度略大,请解释原因 .
(4)E和G形成的某种晶胞如下图所示:其中白球表示E,黑球表示G.则该物质的化学式为 , 假设该晶胞的密度为ρ g/cm3 , 用NA表示阿伏加德罗常数,则该晶胞中距离最近的G原子之间的距离为cm. 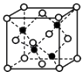
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com