
【题目】为了探究三种气态氧化物(SO2、NO2、CO2)的性质,某同学设计了一组实验:
实验一:探究三种气体在水中的溶解性,用三支相同的试管收集满三种气体,倒置在盛满水的烧杯中,一段时间后,观察到的试管中液面高度如图A、B、C所示.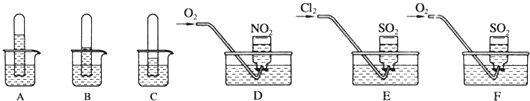
(1)在相同条件下,三种气体在水中溶解度最大的是 , 写出A烧杯中发生反应的化学方程式: .
(2)实验二:用三只集气瓶收集满二氧化硫、二氧化氮气体,然后将其倒置在水槽中.分别缓慢通入适量O2或Cl2 , 如图D、E、F所示.一段时间后,D、E装置的集气瓶中充满溶液,F装置的集气瓶中还有气体剩余.
实验二中装置D的集气瓶最终充满溶液(假设瓶内液体不扩散):
①写出装置D中总反应的化学方程式: ,
②假设该实验条件下,气体摩尔体积为a L/mol,则装置D的集气瓶中所得溶液溶质的物质的量浓度为
(3)实验前在F装置的水槽里滴加几滴紫色石蕊试液,观察到的现象是 , 通入氧气后,可能观察到的实验现象是溶液颜色加深,写出反应的化学方程式:
(4)写出E装置的溶液充满集气瓶时,有关反应的离子方程式 .
【答案】
(1)NO2;3NO2+H2O═2HNO3+NO
(2)4NO2+O2+2H2O═4HNO3;![]() mol/L
mol/L
(3)紫色石蕊试液变红;2SO2+O2+2H2O=2H2SO4
(4)SO2+Cl2+2H2O=4H++SO42﹣+Cl﹣
【解析】解:(1)二氧化硫、二氧化碳的溶解度不大,而二氧化氮水发生氧化还原反应,反应为3NO2+H2O═2HNO3+NO,其溶解度最大;三种气体溶于水得到的溶液均为酸溶液,分别滴几滴紫色石蕊试液,可观察到的现象溶液都变红色,故答案为:NO2;3NO2+H2O═2HNO3+NO;
(2.)①D中二氧化氮、水、氧气反应生成硝酸,反应为4NO2+O2+2H2O═4HNO3 , 故答案为:4NO2+O2+2H2O═4HNO3;②水会充满集气瓶,设集气瓶体积为VL,最后溶液的体积为VL,由4NO2+O2+2H2O═4HNO3知,n(NO2)=n(HNO3),则所得溶液溶质的物质的量浓度为c= ![]() =
= ![]() =
= ![]() mol/L,故答案为:
mol/L,故答案为: ![]() mol/L;
mol/L;
(3.)F装置中二氧化硫与水反应生成亚硫酸,溶液显酸性,滴加几滴紫色石蕊试液,观察到的现象是紫色溶液变红,再通入氧气,发生2SO2+O2+2H2O=2H2SO4 , 酸性增强,红色由浅变深.故答案为:紫色石蕊试液变红;2SO2+O2+2H2O=2H2SO4;
(4.)E装置发生SO2+Cl2+2H2O=H2SO4+2HCl,离子反应为SO2+Cl2+2H2O=4H++SO42﹣+Cl﹣ , 故答案为:SO2+Cl2+2H2O=4H++SO42﹣+Cl﹣ .
(1)二氧化硫、二氧化碳的溶解度不大,而二氧化氮水发生氧化还原反应,其溶解度最大;三种气体溶于水得到的溶液均为酸溶液;(2)①D中二氧化氮、水、氧气反应生成硝酸;②水会充满集气瓶,结合c= ![]() 计算;(3)F装置中二氧化硫与水反应生成亚硫酸,溶液显酸性,再通入氧气,发生2SO2+O2+2H2O=H2SO4 , 酸性增强;(4)E装置发生SO2+Cl2+2H2O=H2SO4+2HCl.
计算;(3)F装置中二氧化硫与水反应生成亚硫酸,溶液显酸性,再通入氧气,发生2SO2+O2+2H2O=H2SO4 , 酸性增强;(4)E装置发生SO2+Cl2+2H2O=H2SO4+2HCl.


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:
【题目】物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。请根据所学的知识回答:
(1)A为0.1 mol/L的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为____________。
(2)B为0.1 mol/L NaHCO3溶液,请分析NaHCO3溶液显碱性的原因:__________________。
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时常加入______溶液以抑制其水解,若把B和C溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程式为__________________。
(4)D为含有足量AgCl固体的饱和溶液,AgCl在水中存在沉淀溶解平衡:AgCl(s)![]() Ag+(aq)+Cl-(aq),在25 ℃时,氯化银的Ksp=1.8×10-10。现将足量氯化银分别放入:①100 mL蒸馏水中;②100 mL 0.2 mol/L AgNO3溶液中;③100 mL 0.1 mol/L氯化铝溶液中;④100 mL 0.1 mol/L盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是___________ (填写序号);②中氯离子的浓度为_______mol/L。
Ag+(aq)+Cl-(aq),在25 ℃时,氯化银的Ksp=1.8×10-10。现将足量氯化银分别放入:①100 mL蒸馏水中;②100 mL 0.2 mol/L AgNO3溶液中;③100 mL 0.1 mol/L氯化铝溶液中;④100 mL 0.1 mol/L盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是___________ (填写序号);②中氯离子的浓度为_______mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关生物体细胞组成元素的叙述,错误的是 ( )
A. 在不同生物的体细胞内,组成它们的化学元素种类大体相同
B. 占人体细胞干重最多的元素为C
C. 在同一生物的不同体细胞内,各种化学元素的含量相同
D. 组成生物体细胞的化学元素,在无机自然界中都能找到
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有着“植物大熊猫”和世界上最长寿树种美称、在地球上已有250万年历史的红豆杉,入选2010年世博会中国馆珍稀植物展出品种。其体内含量最多的化学元素和最基本的化学元素分别是
A. C和O B. C和H C. H和O D. O和C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列有关叙述正确的是( )
A. 标况下,11.2L氟化氢中含有的分子数目为0.5NA
B. 室温下,21.0g乙烯和丁烯的混合气体中所含的碳原子数目是NA
C. 室温下,2L 0.05mol/L的NH4NO3溶液中所含有的氮原子数目是0.2NA
D. 22.4L Cl2与足量NaOH溶液反应时转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】经测定一瓶气体中只含有C、O两种元素,通常情况下这瓶气体不可能是( )
A. 一种化合物 B. 一种单质和一种化合物的混合物
C. 两种化合物 D. 两种单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项表述与示意图形不一致的是

A. 图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1NaOH溶液,溶液pH随加酸体积的变化
B. 图②中曲线表示反应2SO2(g) + O2(g)![]() 2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化
2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化
C. 图③表示10 mL 0.01 mol·L-1KMnO4酸性溶液与过量0.1 mol·L-1草酸溶液混合,n(Mn2+) 随时间的变化
D. 图④中a、b曲线分别表示反应CH2=CH2(g)+ H2(g) →CH3CH3(g);ΔH>0使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,可逆反应X(g)+3Y(g)2Z(g),若X,Y,Z起始浓度分别为c1、c2、c3(均不为0,单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是( )
A.c1:c2=1:3
B.平衡时,Y和Z的生成速率之比为3:2
C.X,Y的转化率不相等
D.c1的取值范围为0<c1<0.14mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com