
科目:高中化学 来源: 题型:
煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应 的热化学方程式如下:
的热化学方程式如下:
CaSO4(s)+CO(g)  CaO(s) + SO2(g) + CO2(g) ΔH1=218.4kJ·mol-1(反应Ⅰ)
CaO(s) + SO2(g) + CO2(g) ΔH1=218.4kJ·mol-1(反应Ⅰ)
CaSO4(s)+4CO(g)  CaS(s) + 4CO2(g) ΔH2= -175.6kJ·mol-1(反应Ⅱ)
CaS(s) + 4CO2(g) ΔH2= -175.6kJ·mol-1(反应Ⅱ)
请回答下列问题:
(1)反应Ⅰ能自发进行的条件是 。
(2)对于气体参与的反应,表示平衡常数Kp时用气体组分(B) 的平衡压强p(B)代替该气体物质的量浓度c(B),则反应Ⅱ的Kp= (用表达式表示)。
的平衡压强p(B)代替该气体物质的量浓度c(B),则反应Ⅱ的Kp= (用表达式表示)。
(3)假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是 。
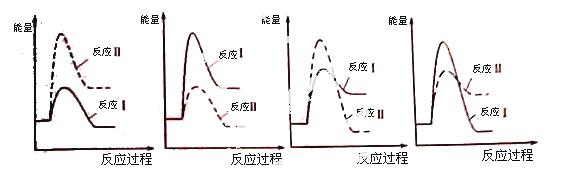
(4)通过监测反应体系中气体浓度的变化判断反应Ⅰ和Ⅱ是否同时发生,理由是 。
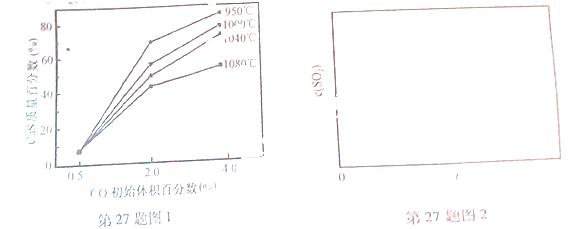
(5)图1为实验测得不同温度下反应体系中CO初始体积百分数与平衡时固体产物中CaS质量百分数的关系曲线。则降低该反应体系中SO2生成量的措施有 。
A.向该反应体系中投入石灰石
B.在合适的温度区间内控制较低的反应温 度
度
C.提高CO的初始体积百分数
D.提高反应体系的温度
(6)恒温恒容条件下,假设反应Ⅰ和Ⅱ同时发生,且v1>v2,请在图2中画出反应体系中c(SO2)随时间t变化的总趋势图。
查看答案和解析>>
科目:高中化学 来源: 题型:
既可以用来鉴别乙烯和甲烷,又可用来除去甲烷中混有的乙烯的方法是
A.通入足量溴的四氯化碳溶液中
B.与足量的液溴反应
C.通入酸性高锰酸钾溶液中
D.一定条件下与H2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下面是化合物Ⅰ(C11H12O3)的合成过程,其分子中含有醛基和酯基。请根据下面所
给条件,回答问题。
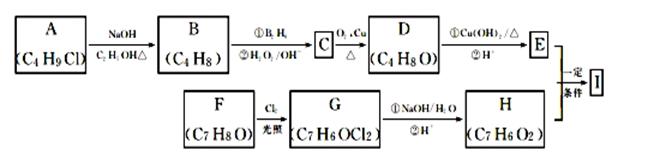
已知以下信息:A的核磁共振氢谱表明其只有一种化学环境的氢;
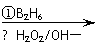 |
RCH=CH2 RCH2CH2OH化合物F苯环上的一氯代物只有两种;通常在
同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。回答下列问题:
(1) A的化学名称为________ _。
(2)F的结构简式是 ;B的结构简式是 ;生成B的反应类型是 。
(3)D生成E的化学方程式为 。
(4)E和H反应生成I的方程式为__________ 。
(5)I的同系物J比I相对分子质量小14,J的同分异构体中能同时满足如下条件:
①苯环上只有两个取代基
②既能发生银镜反应,又能和饱和NaHCO3溶液反应放出CO2
③发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,写出J的这种同分异构体的结构简式_____ _ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)1 mol KHSO4加热熔化可电离出2NA阳离子 ( )
(2)共价化合物溶于水,分子内共价键被破坏,单质溶于水,分子内共价键不被破坏
( )
(3)共价化合物熔点都低于离子化合物 ( )
(4)分子内共价键越强,分子越稳定,其熔、沸点也越高 ( )
(5)含有阳离子的化合物一定含有阴离子 ( )
(6)含有离子键的物质不可能是单质 ( )
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学键的叙述,正确的是 ( )
A.离子化合物中一定含有离子键
B.单质分子中均不存在化学键
C.氯化氢和氯化钾溶解时破坏的化学键相同(2013·上海,4C改编)
D.含有共价键的化合物一定是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C、D是空气中含量最多的两种元素,D、E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)写出D与E以1∶1的原子个数比形成的化合物的电子式:________。F的原子结构示意图为________。
(2)B、D形成的化合物BD2中存在的化学键为________键(填“离子”或“共价”,下同)。A、C、F三种元素形成的化合物CA4F为________化合物。
(3)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为_________________________________________________。
(4)A、C、D、E的原子半径由大到小的顺序是________(用元素符号表示)。
(5)元素B和F的非金属性强弱,B的非金属性________于F(填“强”或“弱”),并用化学方程式证明上述结论____________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。单质Y和W都可与浓的NaOH溶液反应。下列说法不正确的是( )
A.原子半径:Y>Z>W
B.非金属性最强的元素为W
C.Y的最高价氧化物对应的水化物为强酸
D.XW2分子中各原子最外层电子均达到8电子结构
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com