
【题目】下列做法正确的是( )
A.饮用牛奶和豆浆可以缓解重金属引起的中毒
B.二氧化硅用于制造太阳能电池
C.氨气泄漏时,用湿毛巾捂住口鼻,并尽量向高处去
D.用医疗垃圾中的废塑料生产一次性水杯
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.反应C(s)+CO2(g)=2CO(g);△H>0,在任何条件下均不能自发进行
B.铅蓄电池在放电过程中,溶液的PH值增加
C.常温下,在0.1mol/L氨水中,加入少量NH4Cl晶体,溶液的pH减小
D.温度一定时,水的离子积常数Kw不随外加酸(碱)浓度的改变而改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是生物体细胞内部分有机化合物的概念图,请回答下列问题。
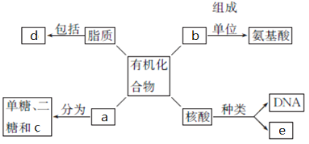
(1)小麦种子中的储能物质c是__________,人和动物细胞中的储能物质c是____________。
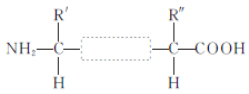
(2)两个氨基酸发生脱水缩合反应时,产物是__________和__________,下图方框内的结构简式是____________。
(3)b结构的多样性决定其功能的多样性,如作为结构物质、免疫功能、___________、___________、信息传递等。
(4)SARS病毒的遗传信息贮存在e中,e物质初步水解的产物是________________;在小麦叶肉细胞中,e主要存在于____________中。
(5)d中构成生物膜的主要是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用MnO2氧化密度为1.19g·cm-3、溶质质量分数为36.5%的HCl溶液。反应方程式如下:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(1)写出该反应的离子方程式______________________________。
(2)该反应的氧化剂为_____________,氧化产物是___________。
(3)17.4gMnO2能与_____摩尔HCl发生上述反应?有______摩尔HCl被氧化?
(4)若在标准状况下产生4.48L Cl2,则反应中转移电子_______摩尔。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水氯化铝是常用的有机化工试剂,易水解、易升华。实验室用以下装置制取少量氯化铝,反应原理为2Al+6HCl(g) ![]() 2AlCl3+3H2。以下说法正确的是
2AlCl3+3H2。以下说法正确的是
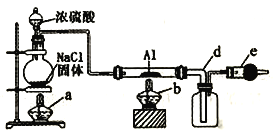
A. 圆底烧瓶中发生反应:NaCl+H2SO4(浓) ![]() HCl↑+NaHSO4
HCl↑+NaHSO4
B. 粗导管d也可换成细导管
C. e中试剂可选用碱石灰、无水氧化钙或五氧化二磷
D. 为了减少HCl的浪费,实验开始时先点燃b处酒精灯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】O2和O3是氧元素的两种单质,根据其分子式完成下列各题:
(1)等质量的O2和O3所含分子个数比为___________,原子个数比为____________,分子的物质的量之比为__________。
(2)等温等压下,等体积的O2和O3所含分子个数比为___________,原子个数比为___________,质量比为__________。
(3)设NA为阿伏加德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积约是__________(用含NA的式子表示)。
(4)实验室中配制2mol·L—1的NaOH溶液950mL,配制时需称取的NaOH的质量是_____________。
(5)在标准状况下15gCO与CO2的混合气体,体积为11.2L混合气体的平均摩尔质量是__________;CO2与CO的体积之比是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。
已知: ① Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O ② SO2+SeO2+ H2O ![]() Se + SO42-+ H+
Se + SO42-+ H+
(1)依据Se与浓H2SO4的反应,写出Se和浓HNO3(还原产物为NO2)反应的化学方程式:__________________。
(2)Se与浓HNO3的反应中,氧化剂是_______, 反应中被还原的元素是_______。当有标准状况下33.6LNO2气体生成时,转移电子的物质的量是________mol。
(3)依据反应①②, 判断SeO2、浓H2SO4、SO2的氧化性由强到弱的顺序是__________。
(4) 配平反应②, 并用双线桥法标出电子转移的方向和数目:_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com