
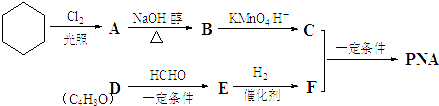
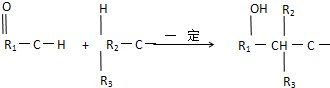
 (R1、R2、R3代表烃基
(R1、R2、R3代表烃基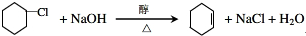 .
. .
. .
. .
.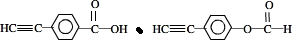 .
.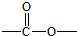 基团
基团分析 由合成图可知,环己烷与氯气光照下发生取代反应生成A,A分子中只有一个氯原子,则A为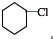 ,然后发生消去反应生成B为
,然后发生消去反应生成B为 ,再被氧化生成C为HOOCCH2CH2CH2CH2COOH,D能发生银镜反应,且分子中有支链,则D为
,再被氧化生成C为HOOCCH2CH2CH2CH2COOH,D能发生银镜反应,且分子中有支链,则D为 ,结合信息②可知,D与HCHO反应生成E为
,结合信息②可知,D与HCHO反应生成E为 ,E与氢气发生加成生成F为
,E与氢气发生加成生成F为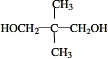 ,C与F发生酯化反应生成PNA为
,C与F发生酯化反应生成PNA为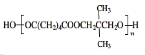 ,据此分析解答.
,据此分析解答.
解答 解:由合成图可知,环己烷与氯气光照下发生取代反应生成A,A分子中只有一个氯原子,则A为 ,然后发生消去反应生成B为
,然后发生消去反应生成B为 ,再被氧化生成C为HOOCCH2CH2CH2CH2COOH,D能发生银镜反应,且分子中有支链,则D为
,再被氧化生成C为HOOCCH2CH2CH2CH2COOH,D能发生银镜反应,且分子中有支链,则D为 ,结合信息②可知,D与HCHO反应生成E为
,结合信息②可知,D与HCHO反应生成E为 ,E与氢气发生加成生成F为
,E与氢气发生加成生成F为 ,C与F发生酯化反应生成PNA为
,C与F发生酯化反应生成PNA为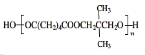 ,
,
(1)A发生消去反应生成B,反应方程式为 ,
,
故答案为: ;
;
(2)C为HOOCCH2CH2CH2CH2COOH,其官能团名称是羧基,故答案为:羧基;
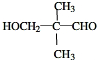
(3)D结构简式为 ,故答案为:
,故答案为: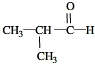 ;
;
(4)E发生加成反应或还原反应生成F,故答案为:加成反应(或还原反应);
(5)E的结构简式为 ,故答案为:
,故答案为: ;
;
(6)C与F在一定条件下生成增塑剂PNA的反应的化学方程式是 ,故答案为:
,故答案为: ;
;
(7)①香豆素是一种重要的香料,与C具有相同的相对分子质量,相对分子质量为146,14.6g香豆素完全燃烧生成39.6g CO2和5.4g H2O,即0.1mol香豆素燃烧生成0.9molCO2和0.3molH2O,再由质量守恒可知,含有氧原子的物质的量为(14.6g-0.9mol×12g/mol-0.6g)÷16g/mol=0.2mol,所以香豆素的分子式是C9H6O2,
故答案为:C9H6O2;
②香豆素的同分异构体符合a.分子中含有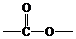 基团;b.分子中除一个苯环外,无其他环状结构;c.苯环上的氢原子被氯原子取代,得到两种一氯代物,则其同分异构体的结构简式为
基团;b.分子中除一个苯环外,无其他环状结构;c.苯环上的氢原子被氯原子取代,得到两种一氯代物,则其同分异构体的结构简式为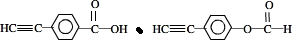 ,
,
故答案为: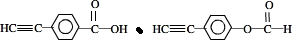 .
.
点评 本题考查有机物的合成,为高频考点,注意有机物的结构和反应条件来推断各物质是解答的关键,利用正推法结合信息即可解答,D、E的转化是解答的难点,题目难度较大.


科目:高中化学 来源: 题型:选择题
| A. | 氧气 | B. | 一氧化碳 | C. | 氮气 | D. | 氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18g≤m≤128g | B. | 36g<m<180g | C. | 18g<m<128g | D. | 36g<m≤180g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯能使酸性高锰酸钾溶液褪色 | |
| B. | 苯能使酸性高锰酸钾溶液褪色 | |
| C. | 乙醇可以和金属钠反应放出氢气 | |
| D. | 乙酸可以与乙醇在一定条件下发生酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 25 | T2 |
| 水的离子积常数 | 1×10-14 | 1×10-12 |
| 难溶物 | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 |
| Ksp | 8.0×10-16 | 8.0×10-38 | 1.0×10-17 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.1 g | B. | 27.2 g | C. | 30 g | D. | 14.6 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3OH的燃烧热为192.9 kJ•mol-1 | |
| B. | CH3OH的燃烧热为676.7 kJ•mol-1 | |
| C. | CH3OH转变成H2的过程一定要吸收能量 | |
| D. | 根据②推知反应:CH3OH(l)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)的△H>-192.9kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com