
【题目】将有铜的印刷线路板浸入200 mL氯化铁浓溶液中,有19.2 g铜被腐蚀掉。取出印刷线路板,向溶液中加入16.8 g铁粉,经充分反应,溶液中还存在9.6 g不溶解的物质。(设溶液体积不变)。请回答下列问题:
(1)充分反应后,溶液中存在9.6 g不溶物的成分为____。
(2)充分反应后溶液中一定不存在的金属离子为_____。
(3)比较Fe2+、Fe3+、Cu2+的氧化性大小:______。
(4)试计算最后溶液中Fe2+的物质的量浓度____mol·L-1。
【答案】Cu Fe3+ Fe3+>Cu2+>Fe2+ 6
【解析】
将有铜的印刷线路板浸入FeCl3浓溶液中,有19.2gCu被腐蚀掉,说明发生反应Cu+2FeCl3=CuCl2+2FeCl2,19.2gCu的物质的量为![]() =0.3mol,则加入铁粉前的溶液中一定含0.3molCuCl2和0.6molFeCl2;
=0.3mol,则加入铁粉前的溶液中一定含0.3molCuCl2和0.6molFeCl2;
(1)加入的16.8 g Fe粉物质的量为![]() =0.3mol,若加入铁粉前溶液中不含FeCl3,则0.3molFe与0.3molCuCl2恰好完全反应生成0.3molCu(即有19.2g不溶物);现有9.6 不溶物,所以不可能为Fe,只能是Cu;故答案为:Cu;
=0.3mol,若加入铁粉前溶液中不含FeCl3,则0.3molFe与0.3molCuCl2恰好完全反应生成0.3molCu(即有19.2g不溶物);现有9.6 不溶物,所以不可能为Fe,只能是Cu;故答案为:Cu;
(2)9.6gCu的物质的量为![]() =0.15mol,根据Cu守恒,溶液中还有0.3mol-0.15mol=0.15molCu2+未反应,Cu能与Fe3+反应生成Fe2+和Cu2+,即Cu与Fe3+不共存,则充分反应后的溶液中一定不存在Fe3+;故答案为:Fe3+;
=0.15mol,根据Cu守恒,溶液中还有0.3mol-0.15mol=0.15molCu2+未反应,Cu能与Fe3+反应生成Fe2+和Cu2+,即Cu与Fe3+不共存,则充分反应后的溶液中一定不存在Fe3+;故答案为:Fe3+;
(3)反应Cu+2FeCl3=CuCl2+2FeCl2中,Fe3+为氧化剂,Cu2+为氧化产物,同一氧化还原反应中氧化性:氧化剂>氧化产物,则氧化性:Fe3+>Cu2+;根据金属活动顺序表,氧化性:Cu2+>Fe2+,所以氧化性由强到弱的顺序为:Fe3+>Cu2+>Fe2+;故答案为:Fe3+>Cu2+>Fe2+;
(4)根据上述分析,加入的铁粉先与氧化性强的Fe3+反应,后与Cu2+发生反应,根据反应Fe+CuCl2=FeCl2+Cu,生成0.15molCu消耗0.15molFe、同时生成0.15molFeCl2;与Fe3+反应的Fe的物质的量为0.3mol-0.15mol=0.15mol,根据反应Fe+2Fe3+=3Fe2+,生成的FeCl2物质的量为0.45mol;则最后溶液中含FeCl2物质的量为0.6mol+0.15mol+0.45mol=1.2mol,则c(Fe2+)=c(FeCl2)=![]() =6mol/L;故答案为:6。
=6mol/L;故答案为:6。


科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是
A.中性溶液中:Fe3+、NH4+、Br、HCO3-
B.澄清透明的溶液中:Na+、Cu2+、NO3-、Cl-
C.c(OH-)<![]() 的溶液中:Na+、Ca2+、ClO-、F-
的溶液中:Na+、Ca2+、ClO-、F-
D.1mo/L的KNO3溶液中:H+、Fe2+、SCN-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个真空恒容密闭容器中盛有1molPCl5,加热到200℃时发生如下反应:PCl5(气) ![]() PCl3(气)+Cl2(气),反应达到平衡时,混合气体中PCl5所占体积分数为M%. 若在同一温度和同一容器中,最初投入是2molPCl5,反应达平衡时,混合气体中PCl5所占体积分数为N%.则M和N的关系 ( )
PCl3(气)+Cl2(气),反应达到平衡时,混合气体中PCl5所占体积分数为M%. 若在同一温度和同一容器中,最初投入是2molPCl5,反应达平衡时,混合气体中PCl5所占体积分数为N%.则M和N的关系 ( )
A. 大于B. 小于C. 等于D. 不能肯定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出)。已知H为固态氧化物,F是红褐色难溶于水的沉淀,且A、B、C、D、E、F六种物质中均含同一种元素。

请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素的名称是________。
(2)反应①的化学方程式为_____________________________________
反应③的离子方程式为________________________
反应⑧的化学方程式为_____________________________________
(3)反应⑥过程中的现象是______________________________。
(4)1molI发生反应后生成的A高温下与足量的水蒸气反应,生成的气体换算成标准状况下占______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室经常用KMnO4与过量浓盐酸反应制备氯气,化学方程式如下:2KMnO4 + 16HCl(浓) = 2KCl + 2MnCl 2+ 5Cl 2↑ + 8H2O。
(1)用单线桥标出电子转移的方向和数目:__________。
(2)将此反应改写为离子方程式:___________________。
(3)若31.6g KMnO4与过量浓盐酸充分反应,被氧化的HCl的物质的量为_____,在标准状况下生成的Cl 2的体积为____。
(4)用生成的氯气通入下面的装置来验证氯气的某些性质。
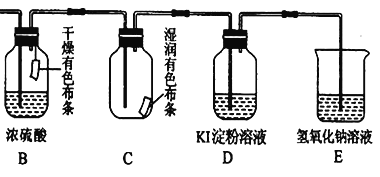
用离子方程式解释C中有色布条褪色的原因:______________,将B、C的顺序颠倒,可否达到原来的实验目的:______(填“可以”或“不可以”);D是用来检验氯气性质的实验,可观察到溶液由无色变为蓝色(I2单质遇淀粉变蓝色),请比较Cl2、I2 、KMnO4 的氧化性,由强到弱为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:

已知:①2KOH+Cl2=KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2=5KCl+KClO3+3H2O(条件:温度较高)
③K2FeO4在水溶液中易水解:4FeO42-+10H2O![]() 4Fe(OH)3(胶体)+8OH-+3O2↑
4Fe(OH)3(胶体)+8OH-+3O2↑
回答下列问题:实验室可利用如图装置完成流程①和②

(1)写出工业上制取Cl2的化学方程式__;两水槽中的水为___(填“热水”或“冷水”)。
(2)反应一段时间后,停止通氯气,再往仪器a中加入浓KOH溶液的目的是___;
A.为下一步反应提供碱性的环境
B.使KClO3转化为 KClO
C.与溶液I中过量的Cl2继续反应,生成更多的KClO
D.KOH固体溶解时会放出较多的热量,有利于提高反应速率
(3)从溶液Ⅱ中分离出 K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子方程式为:___。
(4)用重结晶法提纯粗产品:将粗产品先用KOH稀溶液溶解,再加入饱和的KOH溶液,冷却结晶,过滤,用少量异丙醇洗涤,最后低温真空干燥。
①洗涤粗品时选用异丙醇而不用水的理由是___。
②如何判断 K2FeO4 晶体已经洗涤干净__。
(5)从环境保护的角度看,制备K2FeO4较好的方法为电解法,其装置如图,电解过程中阳极的电极反应式为___。

(6)FeO42-在水溶液中的存在形态如图所示。下列说法正确的是___。

A.不论溶液的酸碱性如何变化,铁元素都有4 种存在形态
B.向pH=10的这种溶液中加硫酸至pH=2,HFeO4-的分布分数逐渐增大
C.向pH=6 的这种溶液中加KOH溶液,发生反应的离子方程式为HFeO4-+OH-=FeO42- +H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2.
已知该反应中H2O2只发生如下过程:H2O2―→O2.
①该反应中的还原剂是____________.
②该反应中,发生还原反应的过程是____________→____________.
③写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目_______
④如反应转移了0.3 mol电子,则产生的气体在标准状况下体积为____________
(Ⅱ)已知实验室利用KMnO4溶液和浓盐酸反应制取Cl2,请回答下列问题:
①配平此化学方程式:
____KMnO4+____HCl(浓)— ____KCl+____MnCl2+____Cl2↑+____H2O
②把此化学方程式改写成离子方程式: ________
③被氧化的HCl 与未被氧化的HCl物质的量之比为____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些氮的化合物是引起大气污染、水体污染和土壤污染原因之一。
I.汽车和工业废气中的氮氧化物是城市空气污染的主要来源。氮氧化物处理通常有下列途径:
(1)在汽车排气管内安装催化转化器,其反应为2NO(g) +2CO(g)= 2CO2(g) +N2(g)。
①该反应能够正向自发进行,则正反应的ΔH_________0(填“>”或“<”)。
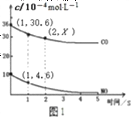
②根据传感器记录某温度下,NO、CO的反应进程,测量所得数据绘制出图1。前1s内平均反应速率v(N2)=__________mol/(L·s);第2s时的X值范围_________________________。
(2)烟气中的氮氧化物(NOx)可与甲烷在一定条件下反应转化为无害成分,从而消除污染。已知
反应 | 反应热(△H/kJ·mol-1) | 平衡常数(K) |
CH4(g)+2O2(g)═CO2(g)+2H2O(l) | a | K1 |
N2(g)+O2(g)═2NO(g) | b | K2 |
则CH4脱硝的热化学方程式为CH4(g) + 4NO (g)![]() CO2(g) + 2N2(g) + 2H2O (l)ΔH=_________kJ/mol(用a、b表示);平衡常数K3=_________(用K1、K2表示)。
CO2(g) + 2N2(g) + 2H2O (l)ΔH=_________kJ/mol(用a、b表示);平衡常数K3=_________(用K1、K2表示)。
II.氰化钠是一种重要的基本化工原料。“天津港”爆炸中,氰化钠产生泄漏,为了避免给土壤和水体带来污染,消防员通过喷洒双氧水来处理泄漏的氰化钠。
(3)已知:NaCN + H2O2+ H2O=NaHCO3+ NH3↑,用H2O2处理1mol NaCN时,反应中转移电子的物质的量为_________mol(NaCN中C为+2价)。
(4)某兴趣小组检测处理后的氰化钠废水是否达标。
已知:①废水中氰化钠的最高排放标准为0.50 mg/L。
②Ag++2CN-= [Ag(CN)2]-,Ag++I-= AgI↓,AgI呈黄色,且CN-优先与Ag+反应。
③实验如下:取30.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.000×10-4mol/L的AgNO3标准溶液滴定,消耗AgNO3溶液的体积为1.50 mL。
④滴定终点的判断方法是_________。
⑤经计算处理后的废水中NaCN的浓度为_________mg/L(保留两位小数),处理后的废水是否达到排放标准:________(填“是”或“否”)
III.工业废水中,含有NaNO2。NaNO2固体外观酷似食盐,误食会中毒。可用电解法将废水中少量的![]() 转化为N2以降低其危害。写出
转化为N2以降低其危害。写出![]() 在酸性条件下转化为氮气的电极反应式为_____________。
在酸性条件下转化为氮气的电极反应式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为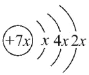 ,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
(1)A为____(写出元素符号,下同);
(2)B为____,简化电子排布式是____;
(3)C为____,核外电子排布式是____;
(4)D为____,轨道表示式是____;
(5)E原子结构示意图是____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com