
| A. | 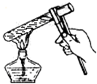 加热试管中的液体 | B. | 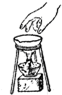 移走蒸发皿 | ||
| C. | 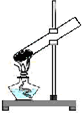 加热结晶水合物 | D. | 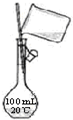 向容量瓶中转移溶液 |
分析 A.试管中液体过多;
B.不能用手拿蒸发皿;
C.结晶水合物分解生成水,会倒流;
D.转移液体用玻璃棒引流,且玻璃棒的下端在刻度线以下.
解答 解:A.试管中液体过多,不能超过试管容积的三分之一,且加热时不能对着自已或别人,故A错误;
B.不能用手拿热的蒸发皿,会烫伤,应利用坩埚钳取蒸发皿,故B错误;
C.结晶水合物分解生成水,会倒流,试管口应略向下倾斜,故C错误;
D.转移液体用玻璃棒引流,且玻璃棒的下端在刻度线以下,图中操作合理,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及实验基本操作和实验细节等,侧重实验能力和实验技能的考查,注意方案的操作性、评价性及实验原理的分析,题目难度不大.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:解答题
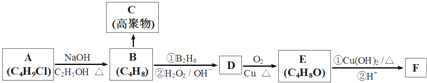
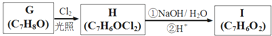
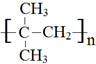 ,
,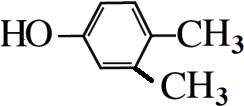 .
.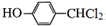 +3NaOH$→_{△}^{水}$
+3NaOH$→_{△}^{水}$ +2NaCl+2H2O.
+2NaCl+2H2O.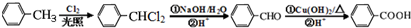 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁和酸反应,放出标准状况下的22.4L气体,转移的电子数必为2NA | |
| B. | 将标准状况下,11.2LN2和33.6LH2混合,在一定条件下充分反应,产生的NH3的分子数为2NA | |
| C. | 常温常压下,6g乙酸所含共价键数目为0.7NA | |
| D. | 1L 0.1mol•L-1碳酸钠溶液中,阴离子数目大于0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子 | 离子浓度(mol•L-1) | |
| 还原前 | 还原后 | |
| Fe2+ | 0.10 | 2.5 |
| SO42- | 3.5 | 3.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
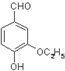 是食品添加剂的增香原料,其香味比香草醛更浓郁.写出乙基香草醛分子中两种含氧官能团的名称醛基、羟基,核磁共振氢谱显示该分子中有7种不同类型的氢原子.
是食品添加剂的增香原料,其香味比香草醛更浓郁.写出乙基香草醛分子中两种含氧官能团的名称醛基、羟基,核磁共振氢谱显示该分子中有7种不同类型的氢原子.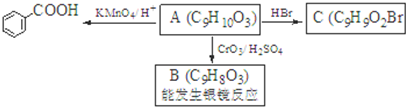
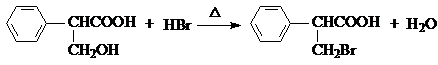 ,属于取代反应(填反应类型).
,属于取代反应(填反应类型). .
. .
. )是一种医药中间体,请设计合理方案用茴香醛(
)是一种医药中间体,请设计合理方案用茴香醛(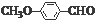 )合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).
)合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
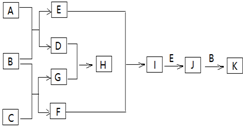 有关物质的转化关系如图所示(部分物质与条件已略去).已知A为淡黄色固体,B为常见的无色液体,C为两种元素组成的化合物,摩尔质量为150g/mol,E为单质气体,F为气态氢化物,有臭鸡蛋气味,G为两性氢氧化物,K为常见的酸.
有关物质的转化关系如图所示(部分物质与条件已略去).已知A为淡黄色固体,B为常见的无色液体,C为两种元素组成的化合物,摩尔质量为150g/mol,E为单质气体,F为气态氢化物,有臭鸡蛋气味,G为两性氢氧化物,K为常见的酸.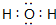 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
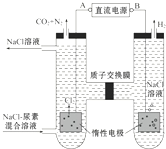
| A. | B为电源的正极 | |
| B. | 电解结束后,阴极室溶液的pH与电解前相比将升高 | |
| C. | 电子移动的方向是B→右侧惰性电极→质子交换膜→左侧惰性电极→A | |
| D. | 阳极室中发生的反应依次为2Cl--2e-=Cl2↑、CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 是天然气的主要成分 | B. | 不能使稀的酸性高锰酸钾溶液褪色 | ||
| C. | 是一种植物生长调节剂 | D. | 是聚乙烯塑料袋的主要成分 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com