
科目:高中化学 来源:不详 题型:单选题
 2COΔH >0 反应速率为V1;N2+3H2
2COΔH >0 反应速率为V1;N2+3H2 2NH3 ΔH﹤0反应速率为V2,对于上述反应,当温度升高时,V1和V2的变化情况为( )
2NH3 ΔH﹤0反应速率为V2,对于上述反应,当温度升高时,V1和V2的变化情况为( )| A.同时增大 | B.同时减少 | C.V1增大,V2减小 | D.V1减小,V2增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| | ① | ② | ④ | ⑤ | ⑥ |
| c(I-)/mol·L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
| c(S2O42-)/mol·L-1 | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t /s | 88.0 | 44.0 | 22.0 | 44.0 | t2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na与无水乙醇反应时增大无水乙醇的用量 |
| B.Zn与25%的稀硫酸反应制取H2时,改用98%的浓硫酸 |
| C.在K2SO4与BaCl2两溶液反应时,增大压强 |
| D.将炭块磨成炭粉用于燃烧 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NO,下列条件能加快其反应速率的是
2NO,下列条件能加快其反应速率的是| A.增大体积使压强减小 | B.体积不变,充入N2使压强增大 |
| C.体积不变,充入He使压强增大 | D.压强不变,充入气体Ne |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
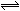 C(s)+4D(g),△H<0。图中a、b曲线表示在一定条件下,D的体积分数随时间的变化情况。若使曲线b变为曲线a,可采取的措施是( )
C(s)+4D(g),△H<0。图中a、b曲线表示在一定条件下,D的体积分数随时间的变化情况。若使曲线b变为曲线a,可采取的措施是( )
| A.升高温度 | B.缩小反应容器的体积 |
| C.增加C的质量 | D.减小B的浓度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③ | B.②③④⑤ | C.①②③④ | D.②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com