
【题目】A为某种聚甲基丙烯酸酯的单体,其转化关系如下:
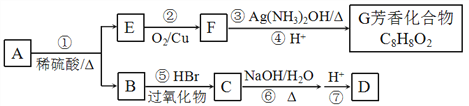
已知:Ⅰ.G的苯环上一氯代物只有两种;Ⅱ.RCH=CH2+HBr![]() RCH2CH2Br
RCH2CH2Br
请按要求回答下列问题:
(1)A的结构简式为____________________。
(2)下列说法不正确的是_______________。
a.②、③、⑤均为氧化反应
b.化合物B分子中所有碳原子共平面
c.化合物C的同系物2-甲基-2-溴丙酸能发生水解、消去、酯化反应
d.用新制碱性氢氧化铜悬浊液可鉴别E、F和G
(3)D可以发生缩聚反应,反应的化学方程式为__________________________________。
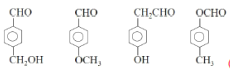
(4)写出同时满足下列条件的G的所有同分异构体的结构简式_____________________。
①红外光谱检测表明分子中含有醛基;
②1H-NMR谱显示分子中含有苯环,且苯环上有两种不同化学环境的氢原子。
以B为原料合成含六元环的酯类物质,请设计合成路线_____________________ (用流程图表示,无机试剂任选)。
【答案】 ![]() ac
ac ![]()
【解析】试题分析:G分子式为C8H8O2,G苯环上一氯代物只有两种,所以G是对甲基苯甲酸;逆推可知,F是对甲基苯甲醛,E是对甲基苯甲醇,A为某种聚甲基丙烯酸酯的单体,则A是![]() ;B是甲基丙烯酸;根据RCH=CH2+HBr
;B是甲基丙烯酸;根据RCH=CH2+HBr![]() RCH2CH2Br,C是BrCH2CH(CH3)COOH、D是HOCH2CH(CH3)COOH;
RCH2CH2Br,C是BrCH2CH(CH3)COOH、D是HOCH2CH(CH3)COOH;
解析:根据以上分析(1)A的结构简式为![]() 。
。
(2)甲基丙烯酸生成BrCH2CH(CH3)COOH属于加成反应,故a错误;
甲基丙烯酸分子中所有碳原子共平面,故b正确;
BrCH2CH(CH3)COOH与 2-甲基-2-溴丙酸是同分异构体,故c错误;
E与新制碱性氢氧化铜悬浊液不反应、F含有醛基能与新制碱性氢氧化铜悬浊液反应生成砖红色沉淀、G含有羧基能与新制碱性氢氧化铜悬浊液发生中和反应,氢氧化铜溶解,故d正确。
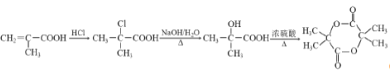
(3)HOCH2CH(CH3)COOH可以发生缩聚反应,反应的化学方程式为![]() 。
。
(4)符合①红外光谱检测表明分子中含有醛基;②1H-NMR谱显示分子中含有苯环,且苯环上有两种不同化学环境的氢原子的甲基苯甲酸的所有同分异构体的结构简式为 。
。
以甲基丙烯酸为原料合成含六元环的酯类物质,合成路线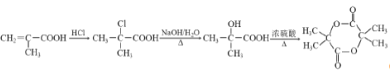


科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的结构的叙述中正确的是( )
A. 除短周期外,其他周期均有18种元素 B. 副族元素中没有非金属元素
C. 周期表中的第三列是ⅢA族 D. 在过渡元素区能找到大量单质半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A的产量是衡量一个国家石油化工发展水平的标志,下图是由A为原料生产某些化工产品的转化关系图。

据此回答下列问题:
(1)写出A分子的结构简式:_________________
(2)写出B、C分子中,含氧基团的名称:B________ C___________
(3)写出下列反应类型:
①_________ ②____________ ③____________
(4)写出下列反应方程式:
②B→CH3CHO:___________________________
③B+C→D:______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关远洋轮船船壳腐蚀与防护叙述错误的是( )
A. 可在船壳外刷油漆进行保护 B. 可将船壳与电源的正极相连进行保护
C. 可在船底安装锌块进行保护 D. 在海上航行时,船壳主要发生吸氧腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G(1,4-环己二醇)是重要的医药中间体和新材料单体,可通过以下流程制备。
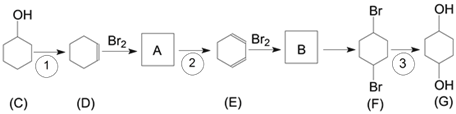
完成下列填空:
(1)写出C中含氧官能团名称_____________。
(2)判断反应类型:反应①_______________;反应③_________________。
(3)写出B的结构简式 _____________________。
(4)一定条件下D脱氢反应得一种产物,化学性质比较稳定,易取代、难加成。该产物属于_________(填有机物类别),说明该物质中碳碳键的特点____________________________。
(5)1,3-丁二烯是应用广泛的有机化工原料,它是合成D的原料之一,它还可以用来合成氯丁橡胶(![]() )。写出以1,3-丁二烯为原料制备氯丁橡胶的单体的合成路线。_________________
)。写出以1,3-丁二烯为原料制备氯丁橡胶的单体的合成路线。_________________
(合成路线常用的表示方式为:![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两烧杯中各盛有100 mL 6 mol/L的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为1:2,则加入铝粉的质量为
A. 10.8g B. 7.2g C. 5.4g D. 3.6g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取溴的工业流程如图:
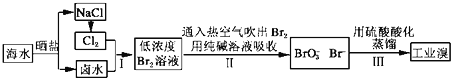
(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是______.
(2)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的______.(填序号)
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)以上流程Ⅱ中涉及的离子反应如下,请在下面方框内填入适当的化学计量数及相应物质:_______
□Br2+□CO32-═□BrO3-+□Br-+□______
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.写出溴与二氧化硫水溶液反应的化学方程式:______.
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是______.(填序号)
A.乙醇 B.四氯化碳 C.烧碱溶液 D.苯.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气系统中的催化转化器,可有效降低尾气中的CO、NO和NO2等向大气排放。在催化转化器的前半部发生的反应为2CO(g) + 2NO(g) ![]() 2CO2(g) + N2(g)。下列说法能充分说明该反应已经达到化学平衡状态的是
2CO2(g) + N2(g)。下列说法能充分说明该反应已经达到化学平衡状态的是
A. CO的转化率100% B. CO、NO、CO2、N2的浓度相等
C. CO、NO、CO2、N2在容器中共存 D. CO、NO、CO2、N2的浓度均不再变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com