
| A. | ③④⑤⑥⑦ | B. | ③④⑥ | C. | ④⑥⑦ | D. | ①③④⑤ |
分析 既能使酸性高锰酸钾溶液褪色,又能使溴的四氯化碳溶液褪色,则有机物中含碳碳双键或三键,或无机物具有还原性,以此来解答.
解答 解:①甲苯只能使高锰酸钾褪色,故不选;
②苯不能使高锰酸钾、溴的四氯化碳溶液褪色,故不选;
③聚乙烯中不含碳碳双键,不能使高锰酸钾、溴的四氯化碳溶液褪色,故不选;
④2-丁炔中含碳碳三键,既能使酸性高锰酸钾溶液褪色,又能使溴的四氯化碳溶液褪色,故选;
⑤环己烷不能使高锰酸钾、溴的四氯化碳溶液褪色,故不选;
⑥1,3-丁二烯中含碳碳双键,既能使酸性高锰酸钾溶液褪色,又能使溴的四氯化碳溶液褪色,故选;
⑦SO2 具有还原性,既能使酸性高锰酸钾溶液褪色,又能使溴的四氯化碳溶液褪色,故选;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意有机物的氧化与加成反应,题目难度不大.


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:选择题
| A. | 每一纵行不是主族就是副族 | |
| B. | 短周期原子的次外层电子数都是8个 | |
| C. | 短周期元素是指原子序数为1~20的元素 | |
| D. | 主族元素所在的族序数等于其原子的最外层电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | v(A)=0.09mol•L-1•s-1 | B. | v(B)=0.06mol•L-1•s-1 | ||
| C. | v(C)=0.9mol•L-1•min-1 | D. | v(D)=3.6mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,将1 mol N2和3 mol H2混合,充分反应后转移的电子数为6NA | |
| B. | 6.4 g由S2、S4、S8组成的混合物含硫原子数为0.2 NA | |
| C. | 0.1mol/LNH4Cl溶液中Cl-离子数为0.1NA | |
| D. | 2.24LNH3和CH4的混合气体,所含电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
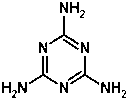 2008年9月11日,全国各地多处发现婴儿因食用三鹿奶粉而出现肾结石的事件.当晚,三鹿集团承认婴幼儿奶粉受到三聚氰胺污染,并宣布召回市面上被污染的产品.三聚氰胺的分子结构如图:有关三聚氰胺的说法正确的是( )
2008年9月11日,全国各地多处发现婴儿因食用三鹿奶粉而出现肾结石的事件.当晚,三鹿集团承认婴幼儿奶粉受到三聚氰胺污染,并宣布召回市面上被污染的产品.三聚氰胺的分子结构如图:有关三聚氰胺的说法正确的是( )| A. | 三聚氰胺属于芳香族化合物,但不属于芳香烃 | |
| B. | 三聚氰胺的分子式为C3N6H6 | |
| C. | 三聚氰胺中的碳原子属于饱和碳原子 | |
| D. | 三聚氰胺分子中的所有原子都在一个平面内 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对氯甲苯、1,2-二氯乙烷、3-甲基-1-丁烯的结构简式分别为: 、CH2Cl-CH2Cl、 、CH2Cl-CH2Cl、 | |
| B. | 2,3,4一三甲基戊烷的核磁共振氢谱中出现四组峰 | |
| C. | 3,4一二甲基己烷的一氯代产物有4种 | |
| D. | 甲苯、硝基苯、2-甲基丙烯分子中的所有碳原子处于同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com