
| A. | A是Zn,B是Cu,C为稀硫酸 | B. | A是Cu,B是Zn,C为稀硫酸 | ||
| C. | A是Fe,B是Ag,C为稀AgNO3溶液 | D. | A是Ag,B是Fe,C为稀AgNO3溶液 |
科目:高中化学 来源: 题型:选择题
| A. | CaC2能水解:CaC2+2H2O═Ca(OH)2+C2H2↑,则Al4C3也能水解:Al4C3+12H2O═4A1(OH)3+3CH4↑ | |
| B. | O2与Cu加热生成CuO,则S与Cu加热生成CuS | |
| C. | 根据化合价Fe3O4可表示为FeO•Fe2O3,则Pb3O4也可表示为PbO•Pb2O3 | |
| D. | SO2通入BaCl2溶液不产生沉淀,则SO2通入Ba(NO3)2溶液也不产生沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
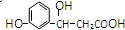 ,它可以发生反应的类型有①加成 ②消去 ③水解 ④酯化 ⑤氧化 ⑥加聚,其中组合完全且正确的是( )
,它可以发生反应的类型有①加成 ②消去 ③水解 ④酯化 ⑤氧化 ⑥加聚,其中组合完全且正确的是( )| A. | ①②③④ | B. | ①②④⑤ | C. | ①②⑤⑥ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某位同学利用家中废旧材料制作了一个可使玩具扬声器发出声音的装置,如图.下列有关该电池工作时的说法正确的是( )
某位同学利用家中废旧材料制作了一个可使玩具扬声器发出声音的装置,如图.下列有关该电池工作时的说法正确的是( )| A. | 木炭棒将逐渐被腐蚀 | |
| B. | 电子流向为铝质汽水罐→导线→食盐水→扬声器→导线→炭棒 | |
| C. | 食盐水中的Na+向炭棒移动 | |
| D. | 炭棒上发生的反应为:2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用明矾使悬浮颗粒沉降下来 | B. | 用漂白粉进行消毒杀菌 | ||
| C. | 只要无色透明,就可以放心饮用 | D. | 饮用前加热煮沸 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
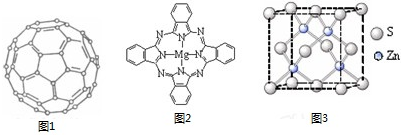
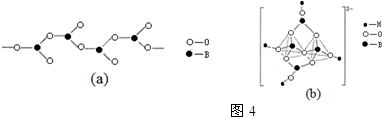
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无单质参加的化合反应有可能是氧化还原反应 | |
| B. | Al既能溶于强酸,又能溶于强碱,所以说明“Al既有金属性,又有非金属性” | |
| C. | 青铜是人类在生产生活中使用最早的合金 | |
| D. | 硅在自然界中只以化合态形式存在 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com