
| A. | Na2SO3溶液(BaCl2) | B. | FeCl2溶液(KSCN) | ||
| C. | 海带灰过滤所得的溶液(淀粉溶液) | D. | NaOH溶液(CaCl2) |
分析 A.Na2SO3溶液变质混有Na2SO4,均与氯化钡反应生成沉淀;
B.FeCl2溶液变质混有FeCl3,可检验铁离子;
C.变质碘离子被生成碘单质;
D.NaOH溶液变质混有碳酸钠,碳酸钠与氯化钙反应生成白色沉淀.
解答 解:A.Na2SO3溶液变质混有Na2SO4,均与氯化钡反应生成沉淀,则加氯化钡不能检验是否变质,故A选;
B.FeCl2溶液变质混有FeCl3,则加KSCN可检验铁离子,能检验是否变质,故B不选;
C.变质混有碘单质,淀粉遇碘单质变蓝,可检验是否变质,故C不选;
D.NaOH溶液变质混有碳酸钠,碳酸钠与氯化钙反应生成白色沉淀,则加氯化钙可检验是否变质,故D不选;
故选A.
点评 本题考查物质的鉴别和检验基本方法及应用,为高频考点,把握变质混有的物质及离子的性质为解答的关键,注意原物质与变质生成的物质反应现象相同不能鉴别,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | +6 | B. | +3 | C. | +2 | D. | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
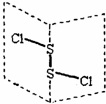 二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体,下列说法中错误的是( )
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体,下列说法中错误的是( )| A. | S2Cl2的结构式为 Cl-S-S-Cl | |
| B. | S2Cl2与水反应时只有S-Cl断裂 | |
| C. | S2Br2含有极性键和非极性键 | |
| D. | S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数为53、中子数为78的碘原子:131 53I | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | 一个D2O分子所含的中子数为8 | |
| D. | N2的电子式:N:::N: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=3的盐酸中,其c(H+)是pH=1的盐酸中的3倍 | |
| B. | 1mol/L0.5L的 AlCl3溶液中,阳离子的物质的量大于0.5mol | |
| C. | 同温度同物质的量浓度时,HF比HCN易电离,则NaF溶液的 pH 比 NaCN 溶液大 | |
| D. | 在由水电离出的c(H+)=1×10-12mol/L的溶液中,K+、ClO-、SO42-一定能大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
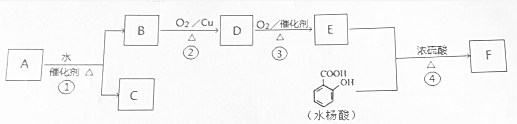
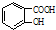 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$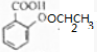 +H2O.
+H2O. $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$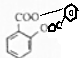 +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com