
| A�� | һ�������£�4.6g NO2��N2O4��������к��е�Nԭ����ĿΪ0.1NA | |
| B�� | 25��ʱ��pH=12��Ba��OH��2��Һ�к��е�OH-��ĿΪ0.01NA | |
| C�� | 1L 0.1mol•L-1 K2CO3��Һ�У���������Ŀ����0.1NA | |
| D�� | 2molSO2��1molO2���ܱ������м��ȣ�V2O5������ַ�Ӧ�������ڷ�����������2NA |
���� A��NO2��N2O4�����ʽ��ΪNO2��
B����Һ�������ȷ��
C��̼�����ˮ��ᵼ�������Ӹ������ࣻ
D����������������ķ�ӦΪ���淴Ӧ�����ܽ��г��ף�
��� �⣺A��NO2��N2O4�����ʽ��ΪNO2����4.6g������к��е�NO2�����ʵ���Ϊn=$\frac{4.6g}{46g/mol}$=0.1mol���ʺ�0.1NA����ԭ�ӣ���A��ȷ��
B����Һ�������ȷ������Һ�е��������ĸ��������㣬��B����
C��̼�����ˮ��ᵼ�������Ӹ������࣬����Һ�е������ӵĸ������࣬��C��ȷ��
D����������������ķ�ӦΪ���淴Ӧ�����ܽ��г��ף���2mol���������1mol������Ӧ�������еķ�����������2NA������D��ȷ��
��ѡB��
���� ���⿼���˰���٤���������йؼ��㣬�������չ�ʽ��ʹ�ú����ʵĽṹ�ǽ���ؼ����ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cl2 | B�� | CaCl2 | C�� | Ca��OH��2 | D�� | Ca��ClO��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
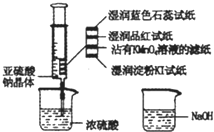 ��ͼ����ע�����м�������Na2SO3���壬��������fŨ���ᣨ�Բ��Ӵ�ֽ��Ϊ�����������й�˵����ȷ���ǣ�������
��ͼ����ע�����м�������Na2SO3���壬��������fŨ���ᣨ�Բ��Ӵ�ֽ��Ϊ�����������й�˵����ȷ���ǣ�������| A�� | ʪ����۵⻯����ֽδ����˵��SO2���ܽ�I-�� ԭΪI2 | |
| B�� | Ʒ����ֽ��մ��KMnO4��Һ����ֽ����ɫ֤����SO2����Ư���� | |
| C�� | ʵ��ɰ�ע�����е���������NaOH��Һ���Լ��ٻ�����Ⱦ | |
| D�� | ��ɫʯ����ֽ�ȱ�����ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
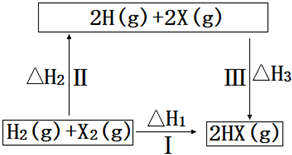
| A�� | 2H��g��+2X��g��=2HX��g����H3��0 | |
| B�� | ;��������HX�ķ�Ӧ����;���أ����ԡ�H1=��H2+��H3 | |
| C�� | ;��������HBr�ų�������������HCl���٣�˵��HBr��HCl�ȶ� | |
| D�� | Cl��Br��I�ķǽ��������μ���������;�������յ��������μ�С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �����£�0.1 mol•L-1 HA��Һ��pH=3����HA�ĵ��룺HA=H++A- | |
| B�� | ��ͭ�缫��ⱥ������ͭ��Һ��2Cu2++2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2Cu+O2��+4H+ | |
| C�� | ��1 mL 2 mol•L-1NaOH��Һ�еμ�1��2��0.1 mol•L-1MgCl2��Һ���ٵμ�2��0.1 mol•L-1 FeCl3��Һ��Mg2++2OH-�TMg��OH��2����3Mg��OH��2+2Fe3+�T2Fe��OH��3+3Mg2+ | |
| D�� | ��������������ʴ�������⣺2Fe+O2+2H2O�T2Fe��OH��2��4Fe��OH��2+O2+2H2O�T4Fe��OH��3��2Fe��OH��3�TFe2O3•xH2O+��3-x��H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
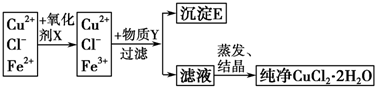
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SiO2��SO2�������������������NaOH��Һ��Ӧ | |
| B�� | Na2O��Na2O2���Ԫ����ͬ����CO2��Ӧ����Ҳ��ͬ | |
| C�� | NO2��CO��NO���Ǵ�����Ⱦ���壬�ڿ����ж����ȶ����� | |
| D�� | ����������Һ��������ҺҪ����ڴ�ĥɰ���������Լ�ƿ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com