


科目:高中化学 来源: 题型:
| A、乙烷的一氯代物同分异构体有1种,二氯代物的同分异构体有3种 |
| B、丙烷的一氯代物同分异构体有2种,二氯代物的同分异构体有5种 |
| C、正丁烷的一氯代物同分异构体有2种,二氯代物的同分异构体有5种 |
| D、正戊烷的一氯代物同分异构体有3种,二氯代物的同分异构体有9种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ④ | ⑦ | ⑨ | |||
| 4 | ② | ⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
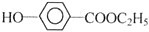
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原电池是把电能转化为化学能的装置 |
| B、一般说来,化学性质较活泼的一极是负极 |
| C、在正极上发生氧化反应 |
| D、在外电路中电子流出的极是正极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com