
已知1gH2燃烧生成液态水时放出142.9kJ的热量,以下热化学方程式正确的是( )
|
| A. | 2H2(g)+O2(g)=2H2O(l)△H=﹣142.9kJ•mol﹣1 |
|
| B. | 2H2(g)+O2(g)=2H2O(l)△H=+571.6kJ•mol﹣1 |
|
| C. | 2H2+O2=2H2O△H=﹣571.6kJ•mol﹣1 |
|
| D. | H2(g)+ |
考点:
热化学方程式.
专题:
化学反应中的能量变化.
分析:
根据热化学方程式的书写判断
书写热化学方程式除了要遵循书写化学方程式的要求外,还应注意以下几方面:
(1)必须注明各反应物、生成物的状态(s、l、g、aq),不标“↑”和“↓”符号.
(2)反应热△H与测定条件(温度、压强)有关,若不说明则指常温(25℃)、常压(101kPa)下.
(3)△H只能写在标有反应物或生成物状态的化学方程式的右边,并用“;”隔开.若为吸热反应,△H为“+”;若为放热反应,△H为“﹣”.△H的单位一般为kJ/mol.
(4)热化学方程式中的化学计量数仅表示该物质的物质的量,不表示物质的分子或原子数,因此可以是整数或分数.
(5)△H与热化学方程式中化学式前面的化学计量数成正比.当反应逆向进行时,其反应热与正反应的反应热数值相等,但符号相反.
(6)书写燃烧热的热化学方程式时,应以燃烧1mol物质为标准来配平其他物质化学式前面的化学计量数.
(7)当两个热化学方程式相加(减)时,反应热同时相加(减),得到一个新的热化学方程式.
解答:
解:A、2mol氢气燃烧生成液态水,放出的热量为142.9kJ×4=571.6kJ,所以△H=﹣571.6kJ•mol﹣1,故A错误;
B、反应为放热反应,△H为“﹣”,故B错误;
C、物质的状态影响反应热,未注明物质的聚集状态,故C错误;
D、1gH2燃烧生成液态水时放出142.9kJ的热量,△H<0,热化学方程式为H2(g)+ O2(g)=H2O(l)△H=﹣285.8kJ•mol﹣1,故D正确.
O2(g)=H2O(l)△H=﹣285.8kJ•mol﹣1,故D正确.
故选:D.
点评:
本题考查热化学方程式,题目难度不大,注意热化学方程式的书写方法.


科目:高中化学 来源: 题型:
橙花醛是一种香料,其结构简式为CH(CH3)2CH2CH2CH2CH(CH3)CH2CHO.下列说法正确的是( )
|
| A. | 橙花醛不能使Br2水褪色 |
|
| B. | 橙花醛能发生银镜反应 |
|
| C. | 1 mol橙花醛最多可以与2 mol H2发生加成反应 |
|
| D. | 橙花醛是丙酮是同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
仔细分析下列表格中烃的排列规律,判断排列在第15位烃的分子式是( )
1 2 3 4 5 6 7 8 9 …
C2H2 C2H4 C2H6 C3H4 C3H6 C3H8 C4H6 C4H8 C4H10
A. C6H12 B. C6H14 C. C7H12 D. C7H14
查看答案和解析>>
科目:高中化学 来源: 题型:
关于 Na2CO3和NaHCO3下列说法不正确的是( )
A. 可以用加热的方法除去Na2CO3中的NaHCO3
B. 分别向Na2CO3和NaHCO3溶液滴加少量盐酸,产生CO2气体较快的为NaHCO3
C. 可以用Ca(OH)2溶液区分Na2CO3和NaHCO3溶液
D. Na2CO3比NaHCO3易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用下面装置测定FeO和Fe2O3固体混合物中Fe2O3的质量,D装置的硬质双通玻璃管中的固体物质是FeO和Fe2O3的混合物.
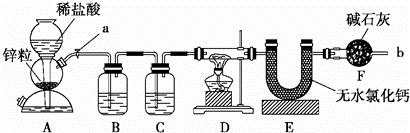
(1)如何检查装置A的气密性?
(2)装置A发生的反应有时要向其中加入少量CuSO4溶液,其目的是
(3)为了安全,在点燃D处的酒精灯之前,在b出口处必须 .
(4)装置B的作用是 ;装置C中装的液体是 .
(5)在气密性完好,并且进行了必要的安全操作后,点燃D处的酒精灯,在硬质双通玻璃管中发生反应的化学方程式是
(6)若FeO和Fe2O3固体混合物的质量为23.2g,反应完全后U型管的质量增加7.2g,则混合物中Fe2O3的质量为 g.
(7)U形管E右边又连接干燥管F的目的是 ,若无干燥管F,测得Fe2O3的质量将 (填“偏大”、“偏小”或“无影响”).
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于平衡常数K的说法中,正确的是( )
|
| A. | 在任何条件下,化学平衡常数是一个恒定值 |
|
| B. | 改变反应物浓度或生成物浓度都会改变平衡常数K |
|
| C. | 平衡常数K只与温度有关,与反应浓度、压强无关 |
|
| D. | 从平衡常数K的大小不能推断一个反应进行的程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图为化学反应:4NH3(g)+5O2(g)⇌4NO(g)+6H2O (g);△H<0 在一密闭容器中反应的v﹣t图.下列叙述不符合如图所给信息的是( )
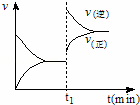
|
| A. | t1时,向容器中通入一定量的NO气体 |
|
| B. | t1时,缩小容器的体积 |
|
| C. | t1时改变外界单一条件时,该反应的平衡常数不一定变化 |
|
| D. | 从t1开始到新的平衡建立的过程中,平衡向逆反应方移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com