
【题目】已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置可以实现该反应。
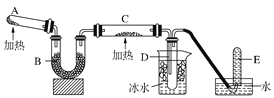
(1)试管A中发生反应的化学方程式是_______________________;
(2)装置B中烧瓶内试剂可选用__(填序号);
a.碱石灰 b.浓硫酸 c.五氧化二磷 d.无水氯化钙
(3)装置C中盛装的物质是___________;实验时在C中观察到的现象是_______;
(4)C中发生的化学反应方程式是________________;
(5)请简述实验室如何验满氨气____________________________________。
【答案】 2NH4Cl+Ca(OH)2== CaCl2+2NH3↑+2H2O a CuO 黑色固体变为红色 3CuO+2NH3 = 3Cu+3H2O+N2(加热条件) 用湿润的红色石蕊试纸检验,试纸变蓝证明有氨气、用玻璃棒蘸浓盐酸或者浓硝酸靠近,产生白烟,证明有氨气。
【解析】(1)根据实验目的:氨与灼热的氧化铜反应得到氮气和金属铜,可知A中加入的是氯化铵和氢氧化钙的固体混合物,加热来制取氨气,发生反应的化学方程式是:2NH4Cl+Ca(OH)2![]() CaCl2+NH3↑+2H2O;
CaCl2+NH3↑+2H2O;
(2)制得的氨气中含有杂质水,可以用碱石灰来吸收,故答案为a;
(3)氨气和氧化铜在加热的条件下发生反应生成金属铜、水以及氮气,黑色粉末逐渐变为红色,发生反应的化学方程式为2NH3+3CuO![]() N2+3H2O+3Cu;
N2+3H2O+3Cu;
(4)根据氨气能与酸反应、其水溶液显碱性,可以用湿润的红色石蕊试纸检验,试纸变蓝证明有氨气或用玻璃棒蘸浓盐酸或者浓硝酸靠近,产生白烟,证明有氨气。


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源: 题型:
【题目】某密闭容器中发生如下反应:X(g)+3Y(g)![]() 2Z(g);ΔH<0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
2Z(g);ΔH<0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
A.t2时加入了催化剂 B.t3时降低了温度
C.t5时增大了压强 D.t4~t5时间内转化率一定最低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E都为短周期元素,A是相对原子质量最小的元素;B的+1价阳离子和C的﹣1价阴离子都与氖原子具有相同的电子层结构;D在C的下一周期,可与B形成BD型离子化合物;E和C为同一周期元素,其最高价氧化物对应的水化物为一种强酸。请根据以上信息回答下列问题:
(1)B元素在元素周期表中的位置是第______周期______族;
(2)画出C元素的原子结构示意图______;
(3)与E的氢化物分子所含电子总数相等的分子是______(举一例,填化学式,下同)、阳离子是______;
(4)A与D形成的化合物中含有化学键的类型是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A. 图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化
B. 图乙表示0.1LpH=2的HC1溶液加水稀释至VL, pH随lgV的变化
C. 图丙表示不同温度下水溶液中H+和OH-浓度变化的曲线,图中温度T2>T1
D. 图丁表示同一温度下,再不同容积的容器中进行反应2BaO2(s)![]() 2BaO(S)+O2(g),O2的平衡浓度与容器容积的关系
2BaO(S)+O2(g),O2的平衡浓度与容器容积的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组设计如图所示实验装置(夹持及控温装置省略),用Cu(NO3)2 3H2O晶体和SOCl2制备少量无水Cu(NO3)2。已知SOC12熔点-l05℃、沸点76℃、遇水剧烈水解生成两种酸性气体。
 .
.
(1)①仪器c的名称是_________________。
②向三颈烧瓶中缓慢滴加SOC12时,需打开活塞_________(选填“a”、“b”或“a 和 b”)。
(2)装置A中Cu(NO3)2 3H2O和SOC12发生反应的化学方程式是________________。
(3)装置B的作用是________________。
(4)实验室以含铁的铜屑为原料制备Cu(NO3)2 3H2O的实验方案如下:
![]()
己知几种离子生成氢氧化物沉淀的pH如下表
开始沉淀的pH | 沉淀完全的pH | |
Fe3+ | 1.1 | 3.2 |
Fe2+ | 5.8 | 8.8 |
Cu2+ | 4.2 | 6.7 |
①步骤I中所用稀HNO3稍过量的目的是_____________。
②请补充完整由溶液I制备Cu(NO3)2 3H2O晶体的实验方案:
向溶液I中加入__________,冰水洗涤得到Cu(NO3)2 3H2O晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是工业上以天然气、空气为原料合成氨的一种工艺流程:

(1)脱硫反应第一步是利用Fe(OH)3除去H2S,该反应的化学方程式是____________。
(2)脱硫反应第二步是利用空气氧化回收硫,该反应中氧化剂与还原剂的物质的量之比为_________,下列试剂中也适宜作此反应的氧化剂的是________(填选项)。
A.Cl2 B.H2O2 C.KMnO4 D.O3
(3)流程中Fe(OH)3和K2CO3可循环利用,你认为流程中还可循环利用的物质有_______。
(4)合成氨反应的原料气中V(N2)∶V(H2)=1∶3。平衡混合物中氨的含量与温度、压强的关系如下图所示:

则A、B、C三点对应的化学平衡常数KA、KB、KC的关系是___________(用“>”、“<”或“=”表示);A点H2的平衡转化率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将1 mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为ΔH1,将1 mol的CuSO4(s)溶于水会使溶液温度升高,热效应为ΔH2;CuSO4·5H2O受热分解的化学方程式为CuSO4·5H2O(s) ![]() CuSO4(s)+5H2O(l),热效应为ΔH3,则下列判断正确的是( )
CuSO4(s)+5H2O(l),热效应为ΔH3,则下列判断正确的是( )
A.ΔH2>ΔH3 B.ΔH1<ΔH3 C.ΔH1+ΔH3=ΔH2 D.ΔH1+ΔH2>ΔH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com