
【题目】某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:

(1)仪器a的名称为______;仪器b中可选择的试剂为______。
(2)实验室中,利用装置A,还可制取的无色气体是______(填字母)。
A.Cl2 B.O2 C.CO2 D.NO2
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体,上述现象证明NH3具有______性,写出相应的化学方程式______。
(4)E装置中浓硫酸的作用______。
(5)读取气体体积前,应对装置F进行的操作:______。
(6)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为n L(已折算成标准状况),则氨分子中氮、氢的原子个数比为______(用含m、n字母的代数式表示)。
【答案】分液漏斗 固体氢氧化钠或氧化钙或碱石灰 BC 还原 3CuO+2NH3![]() 3Cu+3H2O+N2 吸收未反应的氨气,阻止F中水蒸气进入D 慢慢上下移动右边漏斗,使左右两管液面相平
3Cu+3H2O+N2 吸收未反应的氨气,阻止F中水蒸气进入D 慢慢上下移动右边漏斗,使左右两管液面相平 ![]()
【解析】
A装置制取氨气,B装置干燥氨气,C为反应装置,D装置吸收反应产生的水,E装置防止F中的水分进入D装置干扰实验结果,F装置测量生成氮气的体积。
(1)装置中仪器a为分液漏斗,浓氨水遇氧化钙、氢氧化钠会释放氨气,故可选用固体氢氧化钠或氧化钙或碱石灰(成分为氧化钙和氢氧化钠);
(2)该装置为固液不加热制取气体,
A.氯气为黄绿色气体,A错误;
B.过氧化钠和水,或过氧化氢和二氧化锰制氧气都无需加热,B正确;
C.碳酸钙和稀盐酸制取二氧化碳,无需加热,C正确;
D.二氧化氮为红棕色气体,D错误;
答案选BC;
(3)装置C中黑色![]() 粉末变为红色固体,说明氧化铜被还原为铜单质,说明氨气具有还原性,量气管有无色无味的气体,根据元素守恒该气体肯定含有氮元素,只能是氮气,故方程式为
粉末变为红色固体,说明氧化铜被还原为铜单质,说明氨气具有还原性,量气管有无色无味的气体,根据元素守恒该气体肯定含有氮元素,只能是氮气,故方程式为![]() ;
;
(4)根据实验目的,需要测定D装置的质量变化来确定生成水的量,故E装置的作用是防止F中的水分进入D装置,同时浓硫酸还能吸收氨气;
(5)为保证读出的气体体积为标准大气压下的体积,需要调整两边液面相平;
(6)测得干燥管D增重m g,即生成m g水,装置F测得气体的体积为n L,即n L氮气,根据元素守恒,水中的氢元素都来自于氨气,氮气中的氮元素都来自于氨气,故氨分子中氮、氢的原子个数比为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】实验室从含碘废液(除H2O外,含有CCl4、I2、I等)中回收碘,其实验过程如下:
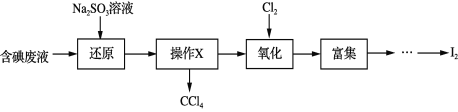
下列叙述不正确的是
A. “操作X”的名称为萃取,可在分液漏斗中进行
B. “还原”步骤发生的反应为:SO32+I2+H2O == 2I+SO42+2H+
C. “氧化”过程中,可用双氧水替代氯气
D. “富集”即I2富集于有机溶剂,同时除去某些杂质离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的制备与工业生产相符的是
①NH3![]() NO
NO![]() HNO3
HNO3
②浓HCl![]() Cl2
Cl2![]() 漂白粉
漂白粉
③MgCl2(aq)![]() 无水MgCl2
无水MgCl2![]() Mg
Mg
④饱和NaCl(aq)![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
⑤铝土矿![]() NaAlO2溶液
NaAlO2溶液![]() Al(OH)3
Al(OH)3![]() Al2O3
Al2O3![]() Al
Al
A.①②⑤B.①④⑤C.②③④D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年南京理工大学合成出下图的离子化合物,该物质由两种阳离子和两种阴离子构成,其中有两种10电子离子和一种18电子离子。X、Y、Z、M均为短周期元素,且均不在同一族。下列说法不正确的是
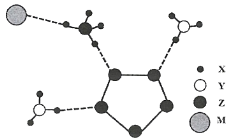
A.X与Y形成的化合物沸点高于Y同族元素与X形成的化合物
B.Z的最高价氧化物对应水化物的酸性比M的强
C.Y气态氢化物的稳定性比Z的强
D.在该盐中,存在极性共价键和非极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一铁的氧化物样品,用140 mL 5 mol·L-1的盐酸恰好完全溶解,所得溶液还能与通入的0.56 L氯气(标准状况)反应,使Fe2+全部转化为Fe3+,则此氧化物为
A.Fe2O3B.Fe3O4C.Fe4O5D.Fe5O7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的恒容密闭容器中,当下列哪些物理量不再发生变化时,表明下述反应:A(s) + 2B(g)![]() C(g) + D(g) 已达到平衡状态‘
C(g) + D(g) 已达到平衡状态‘
①混合气体的压强 ②混合气体的密度
③B的物质的量浓度 ④气体的总物质的量
⑤混合气体总质量
A. ②③⑤ B. ①②③ C. ②③④ D. ①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水化学资源的利用具有非常广阔的前景。以海水为原料制备MgCl2和NaOH的工艺流程如下:
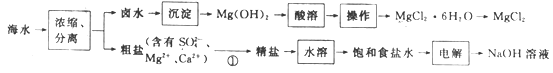
下列说法错误的是
A.“沉淀”时常用石灰乳作为沉淀剂
B.“酸溶”时加入过量盐酸,有利于得到MgCl2·6H2O晶体
C.“电解”时,NaOH在阴极区得到
D.过程①加入试剂的顺序依次为Na2CO3溶液、NaOH溶液、BaCl2溶液、稀盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有X、Y、Z、Q、T五种元素,X原子的M层p轨道有2个未成对电子,Y原子的外围电子构型为3d64s2,Z原子的L电子层的p能级上有一空轨道,Q原子的L电子层的p能级上只有1对成对电子,T原子的M电子层上p轨道半充满。试回答下列问题:
(1)X的元素符号__________,Y的元素符号________。
(2)Z元素原子的电子排布式_______,Q元素原子的电子排布图__________,T元素原子的电子排布图_______________________________。
(3)Y的单质在Q的单质中燃烧的化学方程式:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组在实验室使用软锰矿(主要成分为MnO2)和浓盐酸通过加热制备氯气,并对氯气的性质进行探究。
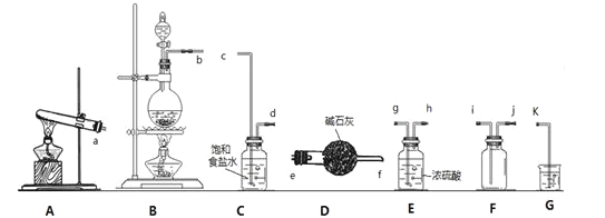
(1)写出实验室制氯气的化学方程式:__。欲制取并收集一瓶于燥的氯气,则“制取→收集”的实验装置连接顺序为__→c→d→__→i→j→k。
(2)装置C中饱和食盐水的作用是___。
(3)该小组同学对氯气性质进行如下探究:
实验步聚 | 实验结论 |
①将氯气通入NaCl溶液中,再加入1mLCCl4振荡,静置,观察四氢化碳层颜色 | 氧化性从强到弱的顺序:氯、溴、碘 |
②将氯气通入KBr溶流中,再加入1mLCCl4振落,静置,观察四氯化碳层颜色 | |
③将氯气通入KI溶液中,再加入1mLCCl4振荡,静置,观察四氧化碳层颜色 |
该小组的实验设计缺陷是___,改进的办法是__。
(4)常温下,高锰酸钾固体和浓盐酸反应也可制得氯气,该反应的离子方程式为:___。
(5)某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-与ClO3-的浓度之比为1:3,则Cl2与NaOH溶液反应时被还原的氯元素与被氧化的氯元素的质量之比为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com