
在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:
Ni(s)+4CO(g) Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表:
| 温度℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法正确的是( )
A.上述生成Ni(CO)4(g)的反应为吸热反应
B.25 ℃时反应Ni(CO)4(g) Ni(s)+4CO(g)的平衡常数为0.5
Ni(s)+4CO(g)的平衡常数为0.5
C.在80 ℃时,测得某时刻,Ni(CO)4、CO浓度均0.5 mol·L-1,则此时v(正)>v(逆)
D.80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol·L-1
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
某有机化合物A的结构简式如下:
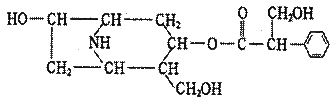
请回答下列问题:
(1)A的分子式是 。
(2)A在NaOH溶液中加热反应得到B和C,C分子中含有苯环。B的结构简式是 。
(3)室温下,C用稀盐酸酸化得到E,E的结构简式是 。
(4)在下列物质中,能与E发生化学反应的是(填写序号) 。
①溴水 ②FeCl3溶液 ③Na2CO3溶液 ④丁烷
(5)写出在铜作催化剂时,E与氧气反应的化学方程式:
。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是分别位于第2、3周期的元素,原子序数依次递增。X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14。下列说法正确的是
A.原子半径由小到大的顺序:X< Y < Z< W
B.Z的最高价氧化物能与水反应生成相应的酸
C.Y单质在一定条件下可以与氧化铁发生置换反应
D.室温下,0.1 mol/L W的气态氢化物的水溶液的pH > 1
查看答案和解析>>
科目:高中化学 来源: 题型:
在一种酸性溶液中,可能存在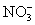 、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,则以下的推测中不正确的是( )
、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,则以下的推测中不正确的是( )
A.一定有碘离子 B.可能含铁离子
C.可能有氯离子 D.不含硝酸根离子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于平衡常数的说法正确的是( )
A.在平衡常数表达式中,反应物浓度用起始浓度,生成物浓度用平衡浓度
B.在任何条件下,化学平衡常数是一个恒定值
C.平衡常数的大小与温度、浓度、压强、催化剂等无关
D.从平衡常数的大小可以推断一个反应进行的程度
查看答案和解析>>
科目:高中化学 来源: 题型:
设反应①Fe(s)+CO2(g) FeO(s)+CO(g)
FeO(s)+CO(g)
ΔH=Q1的平衡常数为K1,反应②Fe(s)+H2O(g) FeO(s)+H2(g) ΔH=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
FeO(s)+H2(g) ΔH=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
| 温度(T) | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1 173 | 2.15 | 1.67 |
(1)从上表可推断,反应①是_______(填“放”或“吸”)热反应;
(2)现有反应③H2(g)+CO2(g) CO(g)+H2O(g) ΔH=Q的平衡常数为K3。
CO(g)+H2O(g) ΔH=Q的平衡常数为K3。
Ⅰ.根据反应①与②推导出K1、K2、K3的关系式K3=______;可推断反应③是______(填“放”或“吸”)热反应。要使反应③在一定条件下建立的平衡右移,可采取的措施有____________________。
A.缩小容器体积 B.降低温度 C.使用合适的催化剂 D.设法减少CO的量
E.升高温度
Ⅱ.根据反应①与②推导出Q1、Q2、Q3的关系式Q3=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是 ( )
A.Na2CO3溶液显碱性: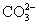 +2H2O
+2H2O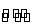 H2CO3+2OH-
H2CO3+2OH-
B.碳酸氢钠溶液中加入足量的烧碱溶液: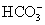 +OH-====
+OH-====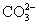 +H2O
+H2O
C.金属钠与水反应:Na+H2O====Na++OH-+H2↑
D.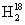 O中投入Na2O2:2
O中投入Na2O2:2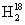 O+2Na2O2====4Na++4OH-+18O2↑
O+2Na2O2====4Na++4OH-+18O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
汉代器物上的颜料“汉紫”至今尚没有发现其自然存在的记载。20世纪80年代科学家进行超导材料研究时,偶然发现其成分为紫色的硅酸铜钡(化学式:BaCuSi2Ox,Cu为+2价),下列有关“汉紫”的说法中不正确的是( )
A.用盐的形式表示:BaSiO3·CuSiO3
B.用氧化物形式表示:BaO·CuO·2SiO2
C.易溶于强酸、强碱
D.性质稳定,不易褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com