


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
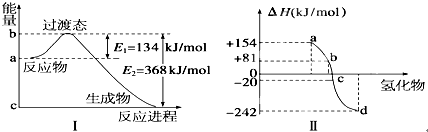
查看答案和解析>>
科目:高中化学 来源: 题型:
 出该加聚反应的化学方程式(可不写反应条件)
出该加聚反应的化学方程式(可不写反应条件)查看答案和解析>>
科目:高中化学 来源: 题型:
 下图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体,化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①式化工生产中的一种重要固氮反应.
下图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体,化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①式化工生产中的一种重要固氮反应.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、未加入稀盐酸之前:c(HCN)>c(Na+)>c(CN-)>c(OH-)>c(H+) |
| B、加稀盐酸后溶液中c(HCN)+c(CN-)=c(Na+) |
| C、PH=7时,溶液中:c(CN-)=c(Na+) |
| D、加稀盐酸后H2O的电离程度减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡向逆反应方向移动 |
| B、达新平衡时,c(N2)较原平衡变小 |
| C、达新平衡时,混合气体的密度变小 |
| D、达新平衡时正、逆反应速率均比原平衡变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径A>B>C |
| B、元素的非金属性C>B>A |
| C、原子的得电子能力B>A>C |
| D、电子层数A=C>B |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com