
在Cu2S+2Cu2O 6Cu+SO2↑反应中,说法正确的是( )
6Cu+SO2↑反应中,说法正确的是( )
|
| A. | Cu2O在反应中被氧化 |
|
| B. | Cu2S在反应中既是氧化剂又是还原剂 |
|
| C. | Cu既是氧化产物又是还原产物 |
|
| D. | 若反应中转移12mol电子,则生成6molCu |
| 氧化还原反应.. | |
| 专题: | 氧化还原反应专题. |
| 分析: | Cu2S+2Cu2O |
| 解答: | 解:A.Cu2O中Cu元素由+1价降低为0价,所以氧化亚铜得电子被还原,故A错误; B.因Cu2S中Cu元素由+1价降低为0价,S元素由﹣2价升高到+4价,则Cu2S既是氧化剂又是还原剂,故B正确; C.Cu元素由+1价降低为0价,则Cu为还原产物,故C错误; D.由反应可知,生成6molCu转移电子数为6mol,则反应中转移12mol电子,则生成12molCu,故D错误; 故选B. |
| 点评: | 本题考查氧化还原反应,明确反应中元素的化合价的变化是解答本题的关键,题目难度不大. |


科目:高中化学 来源: 题型:
化学在环境保护中起着十分重要的作用。催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。
(1)催化反硝化法中,H2能将NO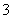 还原为N2。25 ℃时,反应进行10 min,溶液的pH由7变为12。
还原为N2。25 ℃时,反应进行10 min,溶液的pH由7变为12。
①N2的结构式为________。
②上述反应离子方程式为________________,其平均反应速率v(NO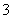 )为________mol·L-1·min-1。
)为________mol·L-1·min-1。
③还原过程中可生成中间产物NO ,写出3种促进NO
,写出3种促进NO 水解的方法__________________________。
水解的方法__________________________。
(2)电化学降解NO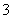 的原理如图所示。
的原理如图所示。
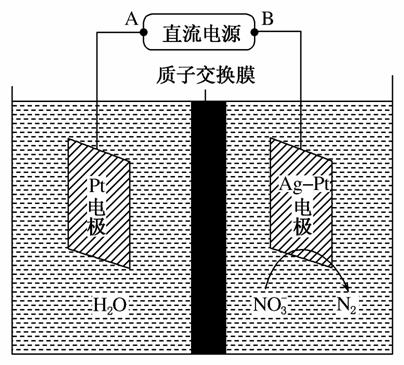
①电源正极为________(填“A”或“B”),阴极反应式为____________。
②若电解过程中转移了2 mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
等质量的①CH4、②H2、③HCl、④SO2,在标准状况下所占体积由大到小排列的顺序是
A ②>①>③>④ B ④>③>①>②
C ③>②>④>① D ①>④>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
三鹿奶粉事件发生后,党中央.国务院高度重视,作出了重大部署,对婴幼儿奶粉进行了三聚氰胺全国专项监督检查,其结果让人震惊。已知三聚氰胺的分子式是C3N6H6,下列有关说法正确的是( )
A.三聚氰胺的摩尔质量为126 g
B.1 mol三聚氰胺的质量为126 g
C.三聚氰胺中N的质量分数为80%
D.1 mol三聚氰胺有15个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
有下列几组反应:
A.Zn+2HCl===ZnCl2+ H2↑ B.CO2+H2O===H2CO3
H2↑ B.CO2+H2O===H2CO3
C.S+O2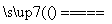 SO2 D.Ba(OH)2+H2SO4===BaSO4↓+2H2O
SO2 D.Ba(OH)2+H2SO4===BaSO4↓+2H2O
E.Na2CO3+2 HCl===2NaCl+H2O+CO2↑ F.CaCO3
HCl===2NaCl+H2O+CO2↑ F.CaCO3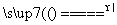 CaO+CO2↑
CaO+CO2↑
G.CH4+2O2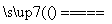 CO2+
CO2+ H2O H.2KClO3
H2O H.2KClO3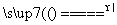 2KCl+3O2↑
2KCl+3O2↑
以上反应中,(1)属置换反应的是________,(2)属化合反应的是________,
(3)属分解反应的是________,(4)属复分解反应的是______,
(5)属氧化还原反应的是___ _____。
_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验过程中,始终无明显现象的是( )
|
| A. | NO2通入FeSO4溶液中 | B. | CO2通入CaCl2溶液中 |
|
| C. | NH3通入AlCl3溶液中 | D. | SO2通入已酸化的Ba(NO3)2溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家最近研究出一种环保、安全的储氢方法,其原理可表示为:储氢释氢NaHCO3+H2 HCOONa+H2O下列有关说法正确的是( )
HCOONa+H2O下列有关说法正确的是( )
|
| A. | 储氢、释氢过程均无能量变化 |
|
| B. | NaHCO3、HCOONa均含有离子键和共价键 |
|
| C. | 储氢过程中,NaHCO3被氧化 |
|
| D. | 释氢过程中,每消耗0.1molH2O放出2.24L的H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数的值,下列说法正确的是
A.标准状况下, 22.4L水含有NA个H2O分子
B.lmol Fe与足量氯气反应时失去的电子数为2NA
C.常温常压下,22. 4LCl2含有2NA个Cl原子
D.32g由氧气和臭氧组成的混合物中含有氧原子的数目为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com