
【题目】氯化亚铁具有独有的脱色能力,适用于染料、染料中间体、印染、造纸行业的污水处理。某课题小组设计如下方案制备氯化亚铁并探究氯化亚铁(Fe2+)的还原性。
某同学选择下列装置用氯化铁制备少量氯化亚铁(装置不可以重复使用)。
查阅资料知:氯化铁遇水剧烈水解,在加热条件下氢气还原氯化铁生成FeCl2和HCl。

(1)实验开始前应先检查装置的气密性,请叙述装置A气密性检验的方法: 。
(2)气流从左至右,装置接口连接顺序是:
a→ ( )→( )→( )→( )→( )
(3)装置C中干燥管中所盛试剂为碱石灰,其作用是: 、
用上述方法制得的氯化亚铁中可能含有氯化铁,某同学设计了如下实验,测定样品中铁元素的质量分数x.请按要求回答下列问题:

(4)反应③的离子方程式为__ ___.
(5)若3次平行滴定实验,平均消耗c mol/L KMnO4溶液的体积为d mL,则样品中铁元素的质量分数(化简代数式)x=_____________;若样品溶解仍使用盐酸而不改用稀硫酸,则所得样品中铁元素的质量分数将(填“偏大”、“偏小”或“无影响”)____ _________.
【答案】(14分)
(1)关闭活塞,向长颈漏斗内注水至形成一段水柱且液面高度不变,说明装置气密性良好
(2)b c e f d
(3)碱石灰或生石灰(1分) 除去HCl、并防止空气中不的进入
(5)2Fe3++Cu=2Fe2++Cu2+
(6)![]() 偏大(1分)
偏大(1分)
【解析】
试题分析:(1)装置气密性的检验,利用长颈漏斗检验使用注水法,加入水形成一段水柱且保持不变,关闭活塞,向长颈漏斗内注水至形成一段水柱且液面高度不变,说明装置气密性良好;
(2)装置的连接顺序是利用装置A生成氢气通过浓硫酸干燥后通入装置D中的玻璃管中加热反应,在加热条件下氢气还原氯化铁生成FeCl2和HCl,剩余氢气通过装置C点燃处理,气流从左至右,装置接口连接顺序是a b c e f d;
(3)装置C中碱石灰或生石灰吸收生成的氯化氢,故C中干燥管应盛放碱石灰作用除去HCl、并防止空气中水的进入;
(4)反应③是加入M把铁离子还原为亚铁离子,最后用高锰酸钾氧化滴定测定亚铁离子的物质的量计算含量,加入的M为铜,反应的离子方程式是2Fe3++Cu=2Fe2++Cu2+;
(5)若3次平行滴定实验,平均消耗c mol/L KMnO4溶液的体积为d mL,物质的量为cmol/L×d×10-3L;依据反应的离子方程式,设亚铁离子物质的量为x:
5Fe2++MnO4-+16H+=Mn2++5Fe3++8H2O
5 1
x cd×10-3mol
x=5 cd×10-3mol
250ml溶液中含铁元素物质的量为5 cd×10-2mol
样品中铁元素的质量分数=![]() ×100%=
×100%=![]() ;
;
若样品溶解仍使用盐酸而不改用稀硫酸,氯离子被高锰酸钾氧化,消耗高锰酸钾物质的量增大,则所得样品中铁元素的质量分数将偏大;


科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、CO32-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图像如图所示。下列说法正确的是( )

A. 原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+
B. 原溶液中一定含有SO42-和Na+
C. 原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
D. 反应最后形成的溶液中含有的溶质为Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10 mL浓度为0.1 mol·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中( )
A. 水的电离程度始终增大
B. ![]() 先增大再减小
先增大再减小
C. c(CH3COOH)与c(CH3COO-)之和始终保持不变
D. 当加入氨水的体积为10 mL时,c (NH4+)=c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人类较早使用的金属之一。据有关报道,目前已经能冶炼出纯度较高的铁。你估计这种“纯铁”不会具有的性质是( )
A.硬度比生铁低
B.熔沸点比生铁高
C.能与Fe2(SO4)3溶液反应
D.不能与盐酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能达到实验目的的是
A. 常温常压下,用铁和浓硫酸制取SO2气体
B. 用酸性高锰酸钾溶液鉴别环己烷和甲苯
C. 用饱和碳酸氢钠溶液除去O2中混有的少量HCl气体
D. 用分液漏斗分离苯和四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知M2O7x-+3S2-+14H+=2M3++3S↓+7H2O,则M2O7x-中的M的化合价为
A. +2价 B. +3价 C. +4价 D. +6价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合图的是
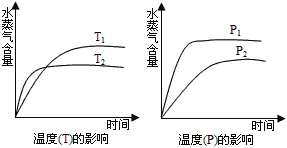
A.CO2(g)+2NH3(g)![]() CO(NH2)2(s)+H2O ΔH<0
CO(NH2)2(s)+H2O ΔH<0
B.CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH>0
CO(g)+H2O(g) ΔH>0
C.CH3CH2OH(g)![]() CH2=CH2(g)+H2O(g) ΔH>0
CH2=CH2(g)+H2O(g) ΔH>0
D.2C6H5CH2CH3(g)+O2(g)![]() 2C6H5CH=CH2(g)+2H2O(g) ΔH<0
2C6H5CH=CH2(g)+2H2O(g) ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面食谱营养搭配最均衡的是
A.凉拌青菜、土豆丝、馒头
B.虾仁白菜、红烧带鱼、酸菜炖猪蹄、萝卜汤
C.糖醋排骨、清蒸鲈鱼、米饭
D.酱牛肉、炒油菜、红烧豆腐、西红柿蛋汤、馒头
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色) ![]() 2CrO42-(黄色)+2H+ 。用K2Cr2O7溶液进行下列实验,结合实验,下列说法不正确的是( )
2CrO42-(黄色)+2H+ 。用K2Cr2O7溶液进行下列实验,结合实验,下列说法不正确的是( )

A. ①中溶液橙色加深,③中溶液变黄 B. ②中Cr2O72-被C2H5OH还原
C. 若向④中加入70%H2SO4溶液至过量,溶液变为橙色 D. 对比②和④可知K2Cr2O7酸性溶液氧化性强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com