
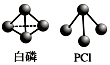
 ��1����úת��Ϊˮú����ͨ����ѧ������úת��Ϊ�ྻȼ�ϵķ���֮һ����֪C��s����CO��g����H2��g����ȫȼ�յ��Ȼ�ѧ����ʽ�ֱ�Ϊ��
��1����úת��Ϊˮú����ͨ����ѧ������úת��Ϊ�ྻȼ�ϵķ���֮һ����֪C��s����CO��g����H2��g����ȫȼ�յ��Ȼ�ѧ����ʽ�ֱ�Ϊ������ ��1����C��s��+O2��g��=CO2��g����H1=-393.5kJ•mol-1
��H2��g��+$\frac{1}{2}$O2��g��=H2O��g����H2=-242.0kJ•mol-1
��CO��g��+$\frac{1}{2}$O2��g��=CO2��g����H3=-283.0kJ•mol-1
�ɸ�˹���ɿ�֪����-��-�۵õ�C��s��+H2O��g��=CO��g��+H2��g����
��2���ʱ���ڷ�Ӧ���м���֮�ͼ�ȥ�������м���֮�ͣ��Դ������
��� �⣺��1����C��s��+O2��g��=CO2��g����H1=-393.5kJ•mol-1
��H2��g��+$\frac{1}{2}$O2��g��=H2O��g����H2=-242.0kJ•mol-1
��CO��g��+$\frac{1}{2}$O2��g��=CO2��g����H3=-283.0kJ•mol-1
�ɸ�˹���ɿ�֪����-��-�۵õ�C��s��+H2O��g��=CO��g��+H2��g�������H=��-393.5kJ•mol-1��-��-242.0kJ•mol-1��-��-283.0kJ•mol-1��=+131.5 kJ•mol-1��
���Ȼ�ѧ����ʽΪC��s��+H2O��g��=CO��g��+H2��g����H=+131.5 kJ•mol-1��
�ʴ�Ϊ��C��s��+H2O��g��=CO��g��+H2��g����H=+131.5 kJ•mol-1��
��2��P4�����ף�s��+6Cl2��g��=4PCl3��s���ķ�Ӧ�ȡ�H=��198kJ•mol-1����6+��243kJ•mol-1����6-��331kJ•mol-1����4��3=-1326 kJ•mol-1��
�ʴ�Ϊ��-1326 kJ•mol-1��
���� ���⿼���Ȼ�ѧ����ʽ��Ϊ��Ƶ���㣬���շ�Ӧ�������仯���ʱ�ļ���Ϊ���ؼ������ط�����Ӧ�������Ŀ��飬ע���˹���ɵ�Ӧ�ã���Ŀ�ѶȲ���


 Сѧѧϰ�ð���ϵ�д�
Сѧѧϰ�ð���ϵ�д� Сѧͬ�����������ܾ�ϵ�д�
Сѧͬ�����������ܾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ƽ���г�����һ���ȷ��0.01g | |
| B�� | ����ƿ�ϱ����¶Ⱥ�������ʹ��ǰҪ����Ƿ�©ˮ | |
| C�� | ����������Һʱ����������Ͳ�м���һ�������ˮ��������עŨ���� | |
| D�� | �����Ȼ�̼�����ͻ�ƾ����л��ܼ������Դӵ�ˮ����ȡ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
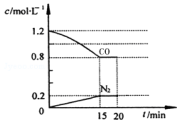 �ش��������⣺
�ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
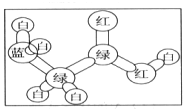 �л��������ǵ��¡�ʳ��ס���м��������зdz����еĹ�ϵ����֪���о��л������ʮ����Ҫ�����ã�
�л��������ǵ��¡�ʳ��ס���м��������зdz����еĹ�ϵ����֪���о��л������ʮ����Ҫ�����ã�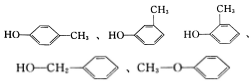 ����дһ�֣���
����дһ�֣����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ʵ����ʵ | �� �� | |
| �� | SO2ʹ���Ը��������Һ��ɫ | ��֤SO2��Ư���� |
| �� | ��ĥ�ڲ���ƿ����NaOH��Һ�����ȵĴ�����Һ�[ϴ�����︽�е����� | ��������������ԭ��Ӧ |
| �� | ȡ����Na2SO3��Ʒ����Ba��NO3��2��Һ������ɫ�������μ�ϡ���ᣬ�������ܽ� | ֤��Na2SO3���������� |
| �� | ij��Һ����ϡ���������ʹ����ʯ��ˮ����ǵ���ɫ��ζ���壬����Һ�μ�CaCl2��Һ���а�ɫ����'���� | ȷ������Һ����CO32- |
| �� | ij��ɫ��Һ�м���Ũ����������Һ�����ȣ�����������ʹʪ���ɫʯ����ֽ���� | ����Һһ����NH4+ |
| A�� | �٢� | B�� | �ۢܢ� | C�� | �ڢ� | D�� | �ܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
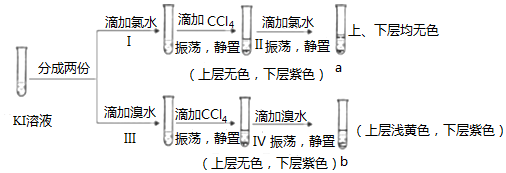
| A�� | CCl4����ȡ������I2������ | |
| B�� | a���²����ɫ��˵��I2 ת��ΪI- | |
| C�� | ���з�����Ӧ�����ӷ���ʽΪ��Br2+2I-�TI2+2Br- | |
| D�� | ֻ����a��b����������֤��Cl2�������Ա� Br2ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ͭ��Һ�м��������NaHS��Һ��Cu2++2HS-�TCuS��+H2S�� | |
| B�� | ��NH4Al��SO4��2��Һ���뺬�������ʵ�����Ba��OH��2��Һ��Al3++2SO${\;}_{4}^{2-}$+4OH-+2Ba2+�T2BaSO4��+AlO${\;}_{2}^{-}$+2H2O | |
| C�� | ��Na2S2O3��Һ��ͨ��������Cl2��S2O${\;}_{3}^{2-}$+2Cl2+3H2O�T2SO${\;}_{3}^{2-}$+4Cl-+6H+ | |
| D�� | ��ʯī�缫���MgCl2��Һ�����缫��Ӧ��2H2O+2e-�TH2��+2OH- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com