
【题目】下列排列顺序不正确的是
A.原子半径:Na>Si>OB.热稳定性:HF>H2O>NH3
C.碱性:CsOH>KOH>NaOHD.失电子能力:Al>Mg>Na
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】在盛有2 mL氯化铁溶液的试管中,加入过量铁粉,振荡试管。充分反应后滴入几滴硫氰化钾溶液,观察到的现象是_________,反应的离子方程式_________;把上层清液倒入另一试管,再加入几滴氯水,又观察到的现象是______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下0.1molL﹣1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是( )
A.将溶液稀释到原体积的10倍
B.加入适量的醋酸钠固体
C.加入等体积0.2molL﹣1盐酸
D.提高溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学选修3:物质结构与性质】铝、铁在生活、生产中有着广泛的用途,请回答下列问题。
(1)Fe2+的最外层电子排布式____________。元素Fe与Mn的第三电离能分别为I3(Fe)、I3(Mn),则I3(Fe)______I3(Mn)(填“>”、“<")。
(2)第四周期中,与Al原子未成对电子数相同的金属元素有____种。气态氯化铝的分子组成为(AlCl3)2,其中Al、Cl均达8e-稳定结构,Al原子的杂化方式为__________。根据等电子原理,AlO2-的空间构型为_____。
(3)Fe(CO)5的熔点为-20℃,沸点为103℃,易溶于乙醚,其晶体类型为______,晶体中σ键和π键的数目之比为______。
(4)科学家们发现某些含铁的物质可催化尿素合成肼(N2H4),沸点:N2H4>C2H6的主要原因为____________。
(5)FeO晶体的晶胞如图所示,己知:FeO晶体的密度为ρg/cm3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为_____;Fe2+与O2-最短核间距为______pm(用ρ和NA表示)。
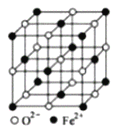
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列描述正确的是( )
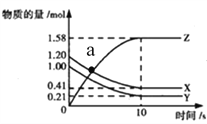
A. 反应的化学方程式为X(g)+Y(g)===Z(g)
B. a点正、逆反应速率相等
C. 反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)
D. 反应开始到10s,Y转化率为79%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体血红蛋白中含有Fe2+离子,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+离子转变成Fe3+离子,生成高铁血红蛋白而丧失与O2结合的能力.服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C具有( )
A.酸性
B.碱性
C.氧化性
D.还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于取代反应的是( )
A.CH2═CH2+HCl ![]() CH3CH2Cl
CH3CH2Cl
B.2CH3CHO+O2 ![]() 2CH3COOH
2CH3COOH
C.![]() +Br2
+Br2 ![]()
![]() ﹣Br+HBr
﹣Br+HBr
D.CH3CH2Br+NaOH ![]() CH2═CH2↑+NaBr+H2O
CH2═CH2↑+NaBr+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向物质的量各有1mol的NH4Al(SO4)2和H2SO4混合稀溶液中逐滴加入一定量Ba(OH)2溶液,产生沉淀的量随着Ba(OH)2 加入量的变化如图所示。下列离子方程式书写正确的是

A. O→A:H++SO42-+Ba2++OH-=BaSO4↓+H2O
B. A→B:2Al3++3SO42-+3Ba2+ +6OH-=3BaSO4↓+2Al(OH)3↓
C. B→C:NH4++SO42-+Ba2+ +OH-=BaSO4↓+NH3·H2O
D. D→E:NH4++ OH-=NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、H、N三种化学元素在组成人体的化学成分中,质量分数共占73%左右,而在组成岩石圈的化学成分中,质量分数还不到1%,这一事实说明了( )
A. 生物界与非生物界具有相似性
B. 生物界与非生物界具有统一性
C. 生物界与非生物界具有差异性
D. 生物界与非生物界的元素组成是不同的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com