
【题目】水的电离平衡曲线如图所示,下列说法不正确的是( )

A.图中五点Kw间的关系B>C>A=D=E
B.若从A点到D点,可采用在水中加入少量酸的方法
C.若处在B点时,将pH=2的硫酸与pH=12的KOH等体积混合后,溶液显碱性
D.若从A点到C点,可用温度不变时在水中加入适量NH4Cl固体的方法
【答案】D
【解析】
A、A、D、E都处于25℃时,Kw相等,B点c(H+)·c(OH-)都大于E点的c(H+)·c(OH-),并且C点的c(H+)·c(OH-)大于A点c(H+)·c(OH-),c(H+)·c(OH-)越大,Kw越大,故B>C>A=D=E,A正确,不符合题意;
B、A点到D点,c(H+)变大,但c(OH-)变小,可加酸,使得c(H+)变大,c(OH-)变小,B正确,不符合题意;
C、若处在B点时Kw=1×10-12,pH=2的硫酸中c(H+)=10-2 mol/L,pH=12的KOH中c(OH-)=1 mol/L,等体积混合,碱过量,溶液呈碱性,C正确,不符合题意;
D、若从A点到C点,c(H+)变大,c(OH-)变大,Kw增大,温度应升高,加入适量的NH4Cl固体,温度不变,则Kw不变,D错误,符合题意;
故合理选项是D。


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】地球化学中,通常用热重分析研究矿物在受热时的质量变化以确定其组成。取66.6 mg由高岭石[Al4Si4O10(OH)8]和方解石(CaCO3)组成的矿物,加热到673K~1123K区间内分解为氧化物,样品总失重13.8 mg。高岭石受热分解反应方程式:Al4Si4O10(OH)8 →2Al2O3+4SiO2+4H2O
(1)硅原子核外电子排布在____个不同的电子层中,核外最外层电子分布在____个不同的轨道中。
(2)硅与铝同周期且相邻,化学性质有相似性,写出Si与NaOH溶液反应的化学方程式________。
(3)高岭石是长石的一种,不同类长石其氧原子的物质的量分数相同。由钙长石化学式CaAl2Si2O8可推知钠长石的化学式为_________________。
(4)此矿物中高岭石的质量分数为____________。
a. 44% b. 56% c. 77.5% d. 80%
(5)若对高岭土进行煅烧活化,然后利用盐酸进行分解,对于分解出的氯化铝溶液及二氧化硅再分别加入碱溶液进行去杂提纯,最后得到的氯化铝溶液可制备氧化铝。写出由氯化铝溶液得到纯净氧化铝的化学反应方程式(要求最节约):_____________________。
(6)用焦炭与石英砂(SiO2)混合高温,产生粗硅,现由两种方法将粗硅提纯:
第一种方法:Si+2Cl2 ![]() SiCl4 SiCl4+2H2
SiCl4 SiCl4+2H2![]() Si+4HCl
Si+4HCl
第二种方法:Si+3HCl ![]() SiHCl3 SiHCl3+H2
SiHCl3 SiHCl3+H2![]() Si+3HCl。
Si+3HCl。
工业上常用第二种方法来提纯单晶硅,其原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述不正确的是( ).
A.在滴有酚酞的 Na2CO3溶液中慢慢滴入BaCl2溶液至过量,溶液的红色褪去
B.往Na2CO3溶液中加水,![]() 增大
增大
C.pH相同的①NH4Cl、②NH4Al (SO4)2、③NH4HSO4三种溶液中c(NH4+):①>②>③
D.在水电离出的c(H+)=1×10-12 mol/L的溶液中,Al3+一定不可能大量存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是重要的化工原料,以乙烯为原料在不同条件下可合成下列物质(部分条件未标出)。完成下列填空:

(1)乙醇能与乙酸反应生成有果香味的物质,其名称为_______,该反应类型是_________。
(2)反应⑥的化学方程式是 _________________,实验现象是 _____________。
(3)反应③用KOH的乙醇溶液处理二氯乙烯的方程式为 ________。
(4)苯乙烯中所含官能团的名称 ____________________。
(5)苯乙烯合成聚苯乙烯的化学方程式是 _______________________。
(6)以乙醇和苯乙烯为原料合成有机物 ,写出合成路线图。______
,写出合成路线图。______
合成路线流程图实例如下:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO、CO2的应用和治理是当今社会的热点问题。CO工业上可用于高炉炼铁,发生如下反应:1/3Fe2O3(s)+CO(g)2/3Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如表:

(1)该反应的正反应为_______反应(填“放热”或“吸热”),欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是___________(选填序号)
a、及时吸收或移出CO2 b、增大反应体系的压强。
c、使用更高效的催化。 d、粉碎矿石增大接触面积
(2)一定条件下,在容积一定的容器中,铁和CO2发生反应:2Fe (s) +CO2 (g)FeO(s) +CO (g) –Q,该反应的平衡常数表达式K=____________。下列措施中能使平衡时c(CO)/c(CO2)增大的是___________(选填编号)。
a.升高温度 b.增大压强
c.充入一定量一氧化碳在 d.再加入一些铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨水是氨气的水溶液,主要用作化肥。现有25℃时0.1 mol/L的氨水,请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中的c(NH4+)_________,溶液的pH_________(填“增大”“减小”“不变”)。
(2)若向氨水中加入稀硫酸,使其恰好中和,写出反应的离子方程式:____________;所得溶液的pH_________7(填“>”、“<”或“=”),用离子方程式表示其原因________。
(3)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子的物质的量浓度由大到小的顺是_______
(4)实验室可用向浓氨水中加入CaO的方法制取氨气,从氨水中存在的平衡入手分析产生NH3的原因:__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既是氧化还原反应,又是吸热反应的是( )
A.铝片与稀硫酸的反应
B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的炭与CO2的反应
D.甲烷在O2中的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某地湖盐中含有Ca2+、Mg2+、Fe3+、SO42-等杂质离子,氨碱厂用该地湖盐制取烧碱。其中制得精制食盐水的过程如下:

(1)过程Ⅰ中将粗盐加水溶解需要适当加热,其目的是__________。
(2)过程Ⅱ的目的是除去SO42-,加入的X溶液是__________。
(3)下表是过程Ⅱ、Ⅲ中生成的部分沉淀及其在20℃时的溶解度[g/100gH2O]
CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 | Fe(OH)3 |
2.6×10-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 | 4.8×10-9 |
①过程Ⅲ中生成的主要沉淀除CaCO3和Fe(OH)3外还有__________。
②过程Ⅳ中调节pH时发生的主要反应的离子方程式为__________。
(4)上述精制食盐水中还含有微量的I-、IO3-、NH4+、Ca2+、Mg2+,除去这些离子及进行电解的流程如下:
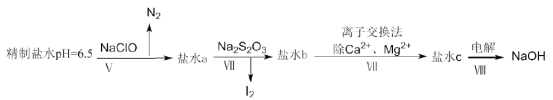
①过程V生成N2的离子方程式为__________。
②过程Ⅳ可以通过控制Na2S2O3的量,将IO3-还原成I2,且盐水b中含有SO42-,该过程中发生氧化还原反应,其中氧化剂和还原剂的物质的量之比为__________。
③在过程Ⅳ中所用的Na2S2O3俗称海波,是一种重要的化工原料。商品海波主要成分是Na2S2O3·5H2O。为了测定其含Na2S2O3·5H2O的纯度,称取8.00g样品,配成250mL溶液,取25.00mL于锥形瓶中,滴加淀粉溶液作指示剂,再用浓度为0.0500mol·L-1的碘水滴定(发生反应2S2O32-+I2=S4O62-+2I-),下表记录滴定结果:
滴定次数 | 滴定前读数(mL) | 滴定后读数(mL) |
第一次 | 0.30 | 29.12 |
第二次 | 0.36 | 30.56 |
第三次 | 1.10 | 29.88 |
计算样品的纯度为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com